根據《海南博鰲樂城國際醫療旅游先行區臨床急需進口藥品管理暫行規定》和《海南自由貿易港博鰲樂城國際醫療旅游先行區臨床急需進口醫療器械管理規定》法規,醫療機構可向衛健委提出特許藥械的申請,經評估確認后可在申請的醫療機構內使用。截至2026年1月,樂城先行區已引進使用特許藥械超過540種,涵蓋腫瘤科、眼科、心血管、康復、醫美、診斷等多個臨床學科,成為全球最新藥械快速進入中國的主要通道。
申報主體:
申請人應為先行區內持有《醫療機構執業許可證》的醫療機構。
評審產品范圍:
申請臨床急需進口的醫療器械為先行區醫療機構因臨床急需,進口已在境外批準上市且在我國尚無同品種產品獲準注冊的醫療器械。
1)用于治療罕見病的醫療器械;用于防治嚴重危及生命疾病且尚無有效治療或者預防手段的醫療器械;用于防治嚴重危及生命疾病且具有明顯臨床優勢的醫療器械;其他經審查符合臨床急需的醫療器械。
2)同品種產品包括:在基本原理、結構組成、制造材料、生產工藝、性能要求、安全性評價、符合的國家/行業標準、預期用途等方面基本等同的已獲境內注冊的產品。在以上方面有重大技術創新,功能性能顯著優于國內已上市產品的除外。
申報流程:
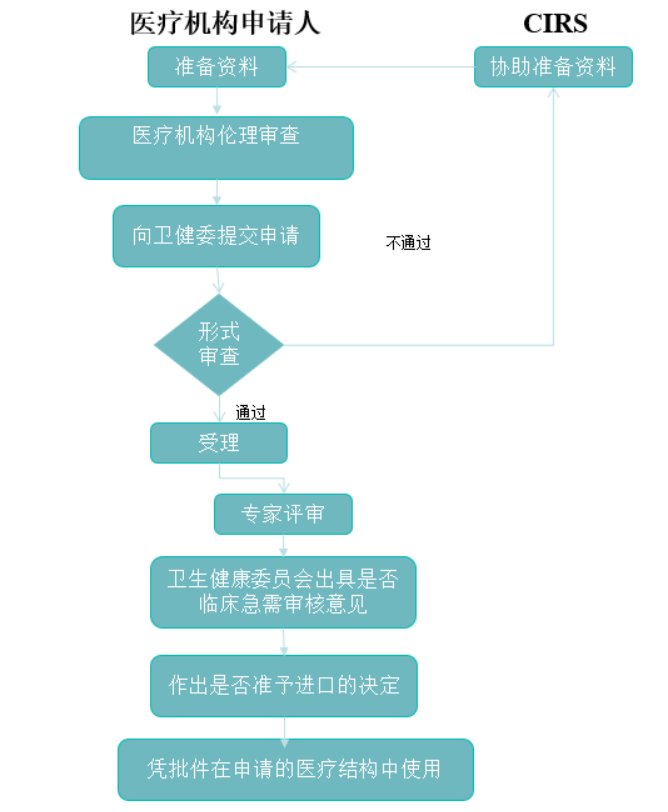
我們的服務:
協助醫療機構準備申請資料
申請資料的提交和跟進
協助企業與醫療機構溝通
附件:同意醫療機構進口臨床急需醫療器械批復(樣表)




