2025年,國家藥監局以習近平新時代中國特色社會主義思想為指導,深入貫徹黨的二十大和二十屆歷次全會精神,全面落實全國藥品監督管理工作會議部署,持續完善支持創新醫療器械發展機制,全方位推進醫療器械審評審批制度改革走深走實,進一步強化醫療器械注冊管理與審評能力建設,以監管效能提升人民群眾用械安全,賦能產業創新高質量發展。
一、醫療器械注冊工作情況
(一)扎實推進醫療器械監管法治建設。2025年,國家藥監局繼續推進《醫療器械管理法》制定,配合市場監管總局推進審查工作。發布《國家藥監局關于進一步調整和優化進口醫療器械產品在中國境內企業生產有關事項的公告》,進一步鼓勵跨國企業在中國境內生產,推動高水平對外開放。發布《關于醫療器械臨床試驗項目檢查要點及判定原則的公告》,細化檢查結果判定方法,明確法律銜接要求,推動臨床試驗項目管理規范化、標準化。發布《醫療器械注冊自檢核查指南》,為自檢核查工作精細化開展提供依據。
(二)著力支持重點領域醫療器械創新突破。2025年,國家藥監局共批準創新醫療器械76個(同比增長17%);優先審批醫療器械25個(同比增長212.5%),獲批產品覆蓋人工智能、腫瘤放射治療、生物醫用材料等多個前沿領域。發布《國家藥監局關于優化全生命周期監管支持高端醫療器械創新發展有關舉措的公告》,以政策集成創新支持高端醫療器械產業發展。研究制定“全球新”醫療器械中國首發工作機制,更加積極主動培育中國造“全球新”。聚焦腦機接口、高端影像設備等核心領域,出臺《優先審批高端醫療器械目錄(2025年版)》。深入調研腦機接口醫療器械研發進展,召開專項工作推進會,匯聚產學研醫管各方資源,加快產品上市進程。專題調度硼中子俘獲治療系統等“國之重器”研發申報進展。聯合推進第二批人工智能醫療器械、生物醫用材料創新任務“揭榜掛帥”工作以及2025年高端醫療裝備推廣應用項目申報工作,加速臨床急需、技術領先的高端醫療器械落地應用。
(三)精準施策有力保障臨床需求。在醫療器械創新研發能力較強的11個省份開展“春雨行動”試點,促進以臨床價值為導向的醫療器械源頭創新和成果轉化。發布《免于進行臨床評價醫療器械目錄(2025年)》《免于進行臨床試驗體外診斷試劑目錄(2025年)》,臨床評價要求更加科學精準。全球首發基孔肯雅病毒檢測試劑標準物質,加速批準基孔肯雅病毒檢測試劑上市。批準7個用于個人自測的甲型/乙型流感病毒抗原檢測試劑盒上市,呼吸道疾病檢測邁向家庭使用新場景。批準8個罕見病診斷試劑,通過精準識別讓有效治療成為可能。支持粵港澳大灣區、海南自貿港等區域建設,指導特許醫療器械使用,惠及患者。
(四)持續規范醫療器械注冊備案管理。繼續開展“進省局、進企業、進醫院,促創新、促規范、促提升”的“三進三促”專題調研,選取代表性省份,全面深入“體檢”省級注冊管理工作。各級監管部門定期發布醫療器械首次注冊備案信息,以公開促規范。國家藥監局發布3期典型備案事例匯編,指導備案實操。加大各省局醫療器械注冊備案數據核查力度,督促提升數據報送質量和效率。發布醫療器械注冊審查指導原則99項,公開審評要點35項。梳理匯總各省第二類醫療器械審評要點,共享2024年境內二類首個醫療器械注冊審評報告,建立各省交流互鑒機制。持續完善注冊管理風險會商機制,國家藥監局每季度開展風險會商,對發現的問題及時通過多種方式實現處置閉環。嚴查注冊造假行為,撤銷提供虛假資料獲取的注冊證等。
(五)縱深推進醫療器械臨床試驗監管。持續加大臨床試驗監督抽查力度,國家藥監局組織開展兩批50個品種的醫療器械臨床試驗監督抽查,現場檢查臨床試驗機構99家次,各地醫療器械臨床試驗機構日常監督檢查實現兩年內全覆蓋,以查促規范,不斷提升醫療器械臨床試驗質量。組織編寫醫療器械臨床試驗監督抽查典型案例匯編,加強臨床試驗檢查工作指導。
(六)加速提升醫療器械審評審批能力。印發《省級醫療器械審評質量管理體系指導意見》,推動全系統審評工作在同一體系下有效開展。組織北京、上海、江蘇、浙江、山東、廣東開展12期線上、6期線下境內第二類醫療器械審評審批實訓,覆蓋近7000人次。舉辦“器審云課堂”44期,新增“器審云課堂”線上中英文培訓視頻189個,發布共性問題答疑77個。
(七)持續健全醫療器械標準體系。2025年,審核報送醫療器械國家標準立項109項,審核發布行業標準80項、廢止14項。現行有效醫療器械標準共2082項,其中國家標準325項,行業標準1757項。“十四五”規劃500項標準制定任務如期完成,標準體系覆蓋性、系統性不斷提升。籌建全國智能化醫療器械、中醫醫療器械標準化工作組,組建醫用光輻射安全和激光設備分技術委員會。加快推動醫用機器人、高端醫學影像設備、人工智能醫療器械、新型生物材料醫療器械、腦機接口醫療器械、中醫器械等重點領域國家標準制定,全球首發2項腦機接口醫療器械標準。積極提升標準領域國際話語權,實質性參與國際標準制修訂。新增國際標準組織注冊專家76名,3項國際標準項目提案獲批立項,牽頭制修訂的國際標準已發布8項、推進中7項。
(八)穩步推進醫療器械分類管理。2025年公開4批次992個典型產品的分類界定結果。開展《醫療器械分類目錄動態調整工作程序》修訂工作。發布《國家藥監局關于調整〈醫療器械分類目錄〉部分內容的公告》。聚焦監管急需,發布二代基因測序相關體外診斷試劑等4個分類界定指導原則,明晰產品注冊申報路徑。研究建立醫療器械分類命名數據庫,完成《醫療器械分類目錄》5926個品名舉例與醫療器械通用名稱的一致性梳理。
(九)不斷提升監管科學化智慧化水平。前瞻性開展腦機接口、人工智能、新型生物材料等醫療器械重點領域10項監管科學項目研究。8家機構成功入圍醫療器械領域監管科學創新研究基地,監管科學研究力量進一步增強。組織9省(市)共同推進人工智能輔助第二類醫療器械注冊審評創新項目,明確人工智能輔助審評應用場景和開發方案。加強臨床試驗信息化建設,指導省局臨床試驗監管信息和項目備案信息填報質量,規范臨床試驗機構年報要求。有序推進醫療器械唯一標識(UDI)實施,研究明確后續品種UDI實施時間表和特定情形UDI實施要求。
(十)積極開展國際交流合作。強化雙邊、深度參與多邊合作,擴展多層次、全方位國際合作網絡。積極參與IMDRF工作,帶領推進GHWP工作,中國醫療器械監管的國際影響力、參與度和領導力得到實質性提升。推動相關國際規則在國內轉化實施,積極推進審評技術要求與國際通用技術要求協調,開展世衛組織WLA認可規則和要求研究,積極推進國際監管信賴,助力中國醫療器械“走出去”。
二、醫療器械注冊申請受理情況
2025年,國家藥監局依職責共受理醫療器械首次注冊、延續注冊和變更注冊申請共計14647項,與2024年相比增加5.9%。
(一)整體情況
受理境內第三類醫療器械注冊申請8766項,受理進口醫療器械注冊申請5881項。
按注冊品種區分,醫療器械注冊申請11106項,體外診斷試劑注冊申請3541項。
按注冊形式區分,首次注冊申請3551項,占全部醫療器械注冊申請的24.24%;延續注冊申請5189項,占全部醫療器械注冊申請的35.43%;變更注冊申請5907項,占全部醫療器械注冊申請的40.33%。注冊形式比例情況見圖1。
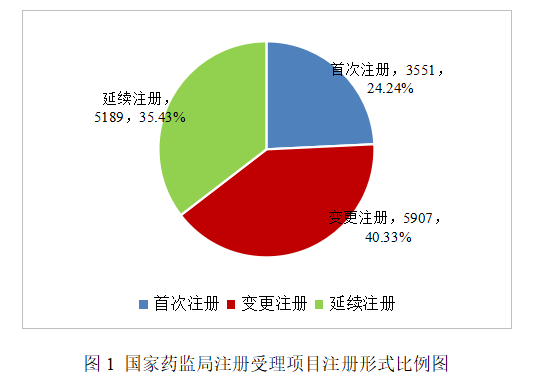
(二)分項情況
1.境內第三類醫療器械注冊受理情況
境內第三類醫療器械注冊受理共8766項,其中醫療器械注冊申請6763項,體外診斷試劑注冊申請2003項。
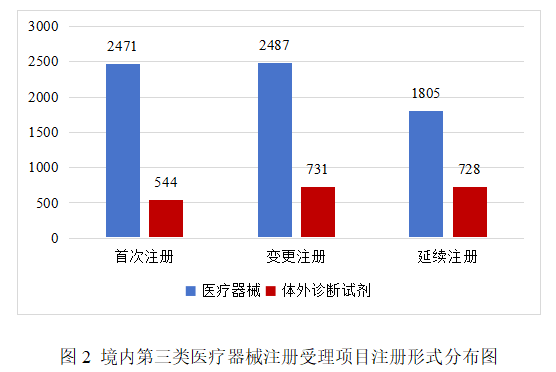
從注冊形式看,首次注冊3015項,占全部境內第三類醫療器械注冊申請數量的34.4%;延續注冊2533項,占全部境內第三類醫療器械注冊申請數量的28.9%;變更注冊3218項,占全部境內第三類醫療器械注冊申請數量的36.7%。注冊形式分布情況見圖2。
2.進口第二類醫療器械注冊受理情況
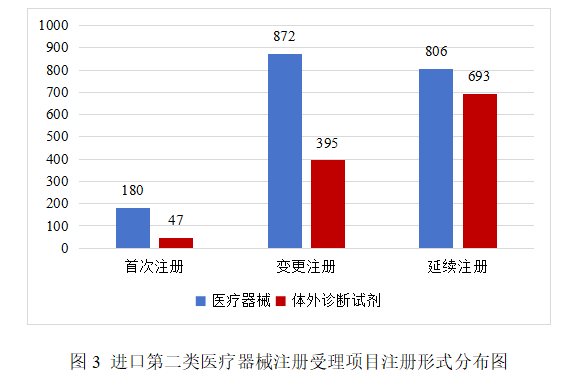
進口第二類醫療器械注冊受理共2993項,其中醫療器械注冊申請1858項,體外診斷試劑注冊申請1135項。
從注冊形式看,首次注冊227項,占全部進口第二類醫療器械注冊申請數量的7.6%;延續注冊1499項,占全部進口第二類醫療器械注冊申請數量的50.1%;變更注冊1267項,占全部進口第二類醫療器械注冊申請數量的42.3%。注冊形式分布情況見圖3。
3.進口第三類醫療器械注冊受理情況
進口第三類醫療器械注冊受理共2888項,其中醫療器械注冊申請2485項,體外診斷試劑注冊申請403項。
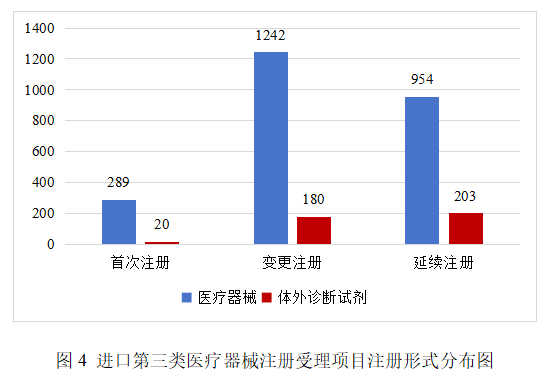
從注冊形式看,首次注冊309項,占全部進口第三類醫療器械注冊申請數量的10.7%;延續注冊1157項,占全部進口第三類醫療器械注冊申請數量的40.1%;變更注冊1422項,占全部進口第三類醫療器械注冊申請數量的49.2%。注冊形式分布情況見圖4。
三、醫療器械注冊審批情況
2025年,國家藥監局共批準醫療器械首次注冊、延續注冊和變更注冊14187項,與2024年相比注冊批準總數量增長8%。
其中,首次注冊3402項,延續注冊5056項,變更注冊5729項。
2025年,企業自行撤回首次注冊申請、自行注銷注冊證書331項。
近12年國家藥監局批準醫療器械注冊情況見圖5。
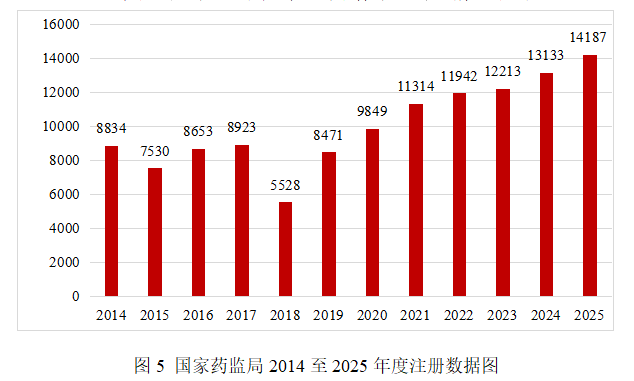
(一)整體情況
2025年,國家藥監局批準境內第三類醫療器械注冊8147項,進口醫療器械6040項。
按照注冊品種區分,醫療器械10621項,占全部醫療器械注冊數量的74.9%;體外診斷試劑3566項,占全部醫療器械注冊數量的25.1%。
按照注冊形式區分,首次注冊3402項,占全部醫療器械注冊數量的24%;延續注冊5056項,占全部醫療器械注冊數量的35.6%;變更注冊5729項,占全部醫療器械注冊數量的40.4%。注冊形式比例情況見圖6。
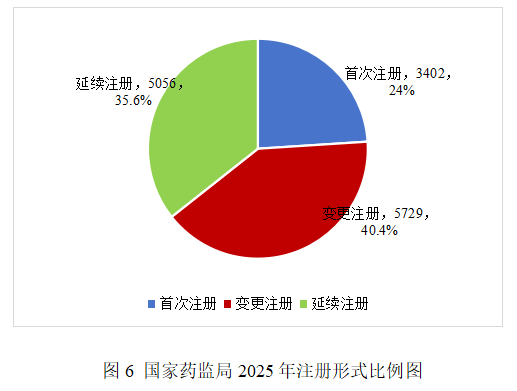
(二)分項情況
1.境內第三類醫療器械注冊審批情況
境內第三類醫療器械注冊8147項。其中,醫療器械6204項,體外診斷試劑1943項。
從注冊形式看,首次注冊2760項,占全部境內第三類醫療器械注冊數量的33.9%,延續注冊2456項,占全部境內第三類醫療器械注冊數量的30.1%;變更注冊2931項,占全部境內第三類醫療器械注冊數量的36.0%。注冊形式分布情況見圖7。
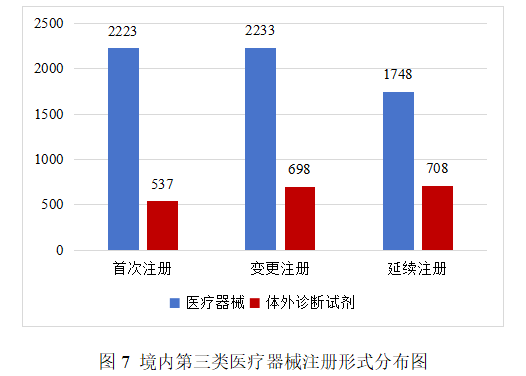
2.進口第二類醫療器械注冊審批情況
進口第二類醫療器械3102項。其中,醫療器械注冊1907項,體外診斷試劑注冊1195項。
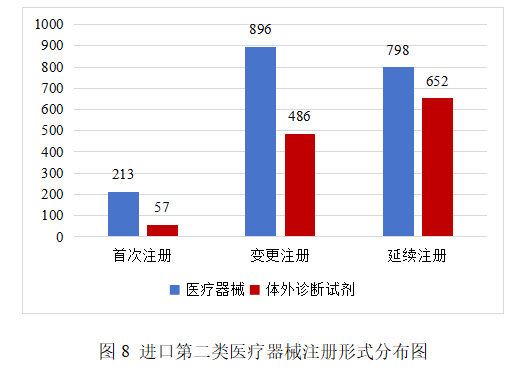
從注冊形式看,首次注冊270項,占全部進口第二類醫療器械注冊數量的8.7%;延續注冊1450項,占全部進口第二類醫療器械注冊數量的46.7%;變更注冊1382項,占全部進口第二類醫療器械注冊數量的44.6%。注冊形式分布情況見圖8。
3.進口第三類醫療器械注冊審批情況
進口第三類醫療器械注冊2938項。其中,醫療器械注冊2510項,體外診斷試劑注冊428項。
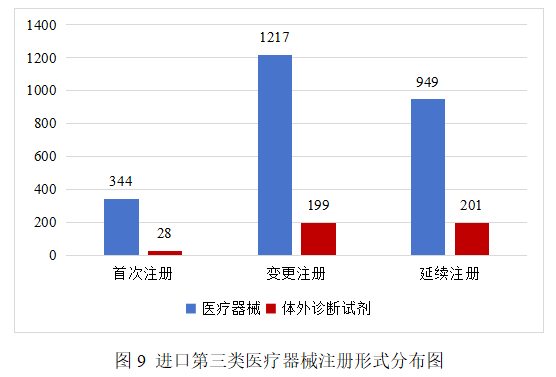
從注冊形式看,首次注冊372項,占全部進口第三類醫療器械注冊數量的12.7%;延續注冊1150項,占全部進口第三類醫療器械注冊數量的39.1%;變更注冊1416項,占全部進口第三類醫療器械注冊數量的48.2%。注冊形式分布情況見圖9。
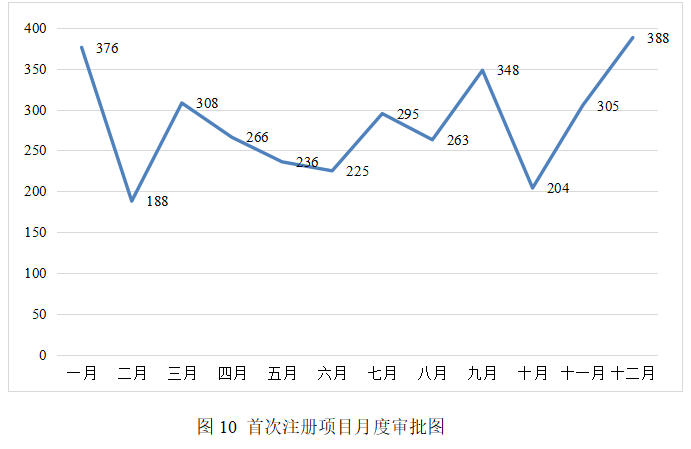
(三)首次注冊項目月度審批情況
2025年,國家藥監局首次注冊月度審批情況見圖10。
(四)具體批準品種種類分析
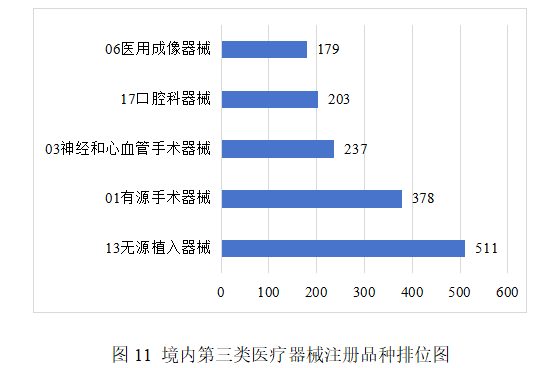
注冊的境內第三類醫療器械,除體外診斷試劑外,共涉及《醫療器械分類目錄》中18個子目錄的產品。
注冊數量前五位的境內第三類醫療器械是:無源植入器械,有源手術器械,神經和心血管手術器械,口腔科器械,醫用成像器械。與2024年相比,無源植入器械注冊數量同比增加5.1%,有源手術器械超過神經和心血管手術器械,注冊數量同比增加34.5%,醫用成像器械超過注輸、護理和防護器械進入前五位,其他品類注冊數量有所下降,如注輸、護理和防護器械同比減少31.9%,神經和心血管手術器械同比減少19.9%,口腔科器械同比減少1%。
注冊的進口醫療器械,除體外診斷試劑外,共涉及《醫療器械分類目錄》中21個子目錄的產品。
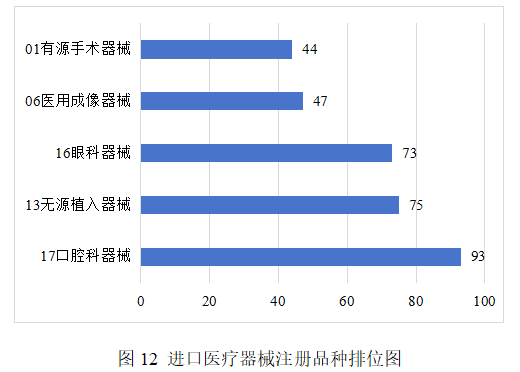
注冊數量前五位的進口醫療器械是:口腔科器械,無源植入器械,眼科器械,醫用成像器械,有源手術器械。與2024年相比,變化較大,口腔科器械超過無源植入器械,位居第一,注冊數量同比增加24%,眼科器械超過有源手術器械,注冊數量同比增加35.2%,醫用成像器械超過有源植入器械進入前五位,其他品類注冊數量略有下降。
(五)進口醫療器械國別情況
2025年,共有30個國家(地區)產品在我國獲批上市。
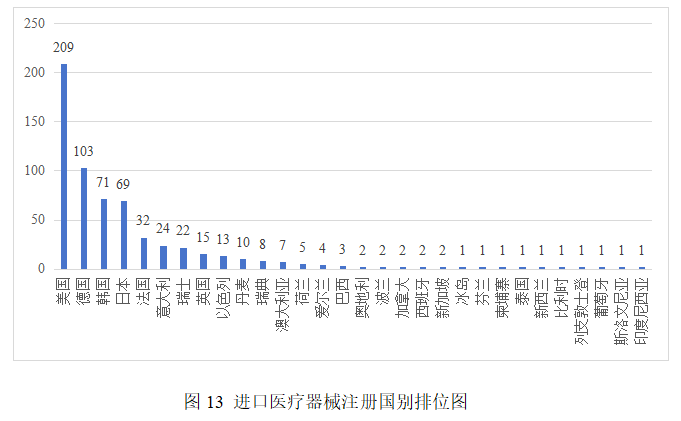
其中,美國、德國、韓國、日本、法國醫療器械在中國醫療器械進口產品首次注冊數量位列前5位,注冊產品數量約占2025年進口產品首次注冊總數量的75.4%。
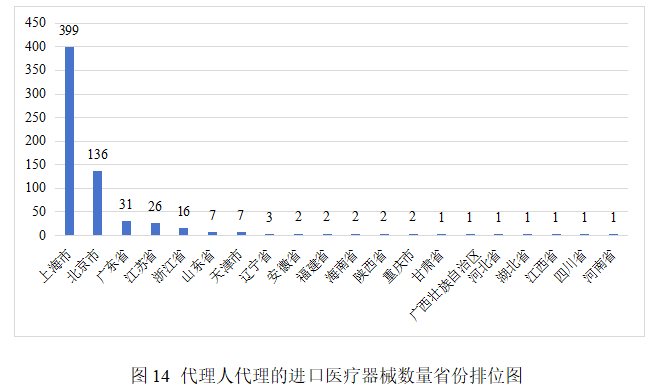
從進口醫療器械代理人分布看,共有19個省涉及有本省企業作為進口醫療器械代理人,其中上海市代理人代理的進口首次醫療器械數量最多,占全部進口醫療器械數量的62.1%。
(六)境內第三類醫療器械省份分析
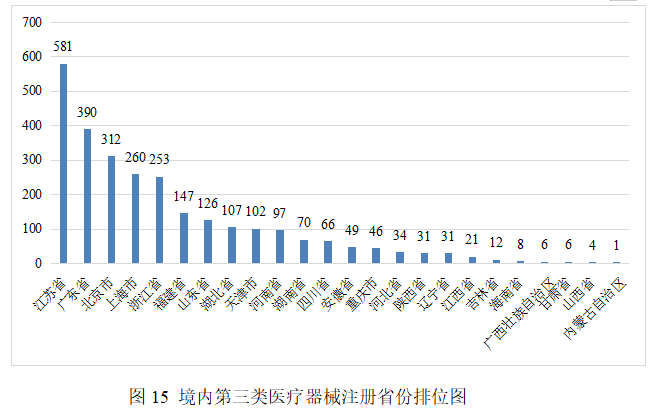
從2025年境內第三類醫療器械注冊情況看,相關注冊人主要集中在沿海經濟較發達省份。
其中,江蘇、廣東、北京、上海、浙江是境內第三類醫療器械首次注冊數量排前五名的省份,占2025年境內第三類醫療器械首次注冊數量的65.1%。
四、創新醫療器械等產品注冊審批情況
2025年,國家藥監局按照《創新醫療器械特別審查程序》《醫療器械優先審批程序》繼續做好相關產品的審查工作,共收到創新醫療器械特別審批申請457項,其中104項獲準進入創新醫療器械特別審查程序;收到優先申請38項,其中26項獲準優先審批。
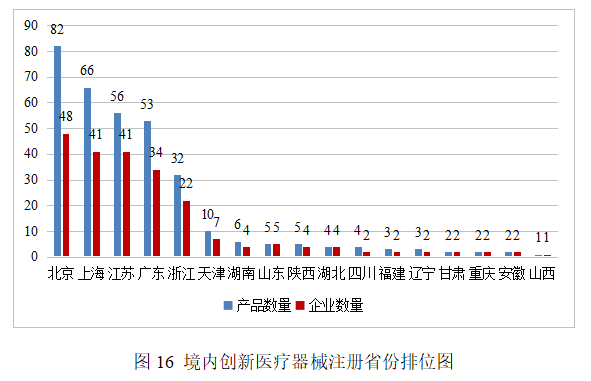
從2014年至2025年,國家藥監局共批準391個創新醫療器械。其中境內創新醫療器械336個,涉及17個省的223家企業;進口創新醫療器械55個,涉及6個國家的30個企業。北京、上海、江蘇、廣東、浙江創新醫療器械獲批產品數量和相應企業數量最多,約占全部已批準的391個創新醫療器械的73.9%。
已批準的創新醫療器械中,有源產品占比約61%,無源產品約32%,體外診斷試劑產品約7%,具體見圖17。
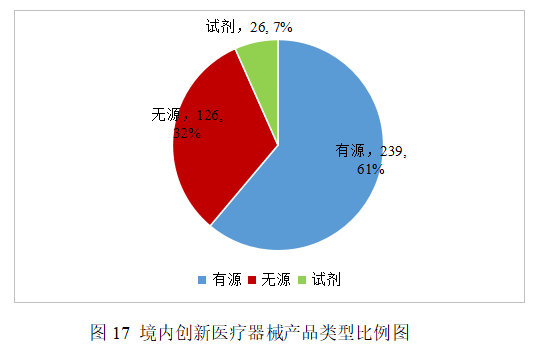
2025年,國家藥監局共批準76個創新醫療器械產品上市,相比2024年增加16.9%。其中有源醫療器械45個,無源醫療器械29個,體外診斷試劑2個。
有源手術器械、無源植入器械、有源植入器械、眼科器械、神經和心血管手術器械是2025年批準的創新醫療器械數量前五位的品類,與2024年相比,無源植入器械和眼科器械品類的創新產品增長較快。具體見圖18。
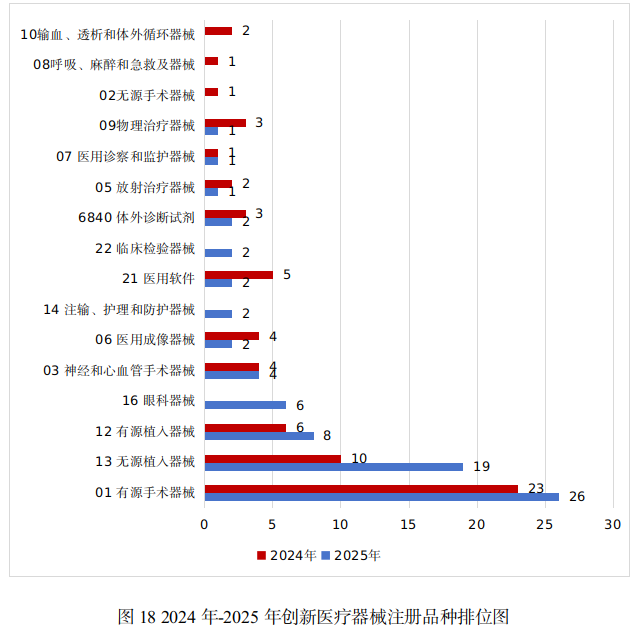
這些創新產品核心技術都有我國的發明專利權或者發明專利申請已經國務院專利行政部門公開,產品主要工作原理/作用機理為國內首創,具有顯著的臨床應用價值。以下是已批準創新醫療器械產品介紹:
(一)有晶體眼人工晶狀體:該產品用于成年人有晶狀體眼的治療,矯正/降低成年人-3.25D-18.00D的近視度數。產品采用零球差大光學區及雙凹面型的穩定拱高設計,可提升視覺質量,帶來更開闊的周邊拱高。
(二)冷凍消融儀:該產品由主機、同軸流體連接管和連接電纜組成,與該公司生產的球囊型冷凍消融導管配合使用,采用壓力流量雙控制技術,通過實時監測和控制制冷劑流量與球囊壓力,實現球囊在充氣和消融過程中的壓力穩定。該技術可有效降低球囊在封堵肺靜脈和消融過程中因壓力波動而產生的彈跳移位風險,用于成人患者藥物難治性、復發性、癥狀性的陣發性房顫治療。
(三)人CDO1/AJAP1/GALR1基因甲基化檢測試劑盒(熒光PCR法):該產品由引物、探針、聚合酶等材料組成,對人宮腔脫落細胞樣本中基因甲基化狀態進行定性檢測,用于疑似子宮內膜癌患者的輔助診斷,對子宮內膜癌的防治、提升患者生存率具有重要意義。
(四)多焦點人工晶狀體:該產品為單件式后房人工晶體,由疏水性丙烯酸酯類材料制成,添加紫外吸收劑,可折疊。適用于成人白內障患者無晶體眼的視力矯正,以期待改善近、中、遠視力并減少眼鏡依賴。
(五)紫杉醇藥物涂層外周球囊導管:該產品為OTW型球囊擴張導管,由遠端尖端、球囊、鎳鈦合金約束結構(CS)、導管軸、應力擴散管、導管座、射線顯影環等組件組成。鎳鈦合金約束結構為球囊外的環狀結構,在軸向和徑向均分布有約束絲。球囊表面涂覆有紫杉醇,涂層輔料為沒食子酸丙酯。產品經環氧乙烷滅菌,一次性使用,貨架有效期6個月。該產品用于在股淺動脈、腘動脈原發狹窄病變的經皮腔內血管成形術治療,病變長度不超過180mm,適用血管直徑范圍為4-7mm,使用該產品前需經充分預擴張。
(六)微衛星不穩定性(MSI)檢測試劑盒(熒光PCR-毛細管電泳法):該產品采用了熒光PCR-毛細管電泳法,通過對結直腸癌患者腫瘤組織基因組中的8個微衛星位點定性檢測,可實現癌組織樣本位點狀態的精準判定。該產品主要用于輔助結直腸癌中可能的林奇綜合征檢測,有利于直腸癌防治、提升患者生存率。
(七)心臟脈沖電場消融系統和一次性使用磁定位心臟脈沖電場消融導管:心臟脈沖電場消融系統由控制臺腳踏開關、連接電纜、電源線等組成,一次性使用磁定位心臟脈沖電場消融導管由環形頭端部(含電極)、導管管身、手柄組成。二者聯合使用,主要用于治療藥物難治性、復發性、癥狀性的陣發性房顫。該產品利用脈沖電場的非熱效應原理進行房顫治療,與傳統的射頻消融及冷凍消融產品相比,可實現對心肌組織的選擇性破壞,避免溫度傳遞導致的周圍組織損傷風險。
(八)經導管二尖瓣夾系統:該產品適用于經心臟團隊評估后認為存在外科手術高風險,且二尖瓣瓣膜解剖結構適合的退行性二尖瓣反流(MR≥3+)患者。產品采用包裹托舉狀的閉合形態設計,預期可以實現植入后穩固的錨定;采用錨固件四通道控制通路設計,能夠實現瓣葉同時或者分別捕獲,預期提高手術成功率,減少手術風險。
(九)主動脈覆膜支架系統:該產品適用于需要重建左鎖骨下動脈血運的Stanford B型夾層患者,其近端錨定區長度應≥15mm。該產品為首款明確適用于煙囪技術的主動脈覆膜支架系統,其主動脈分支支架采用帶外層裙邊的雙層支架結構設計,外層裙邊可在支架釋放后填補支架與血管形成的間隙,預期可以防止和減少內漏發生,降低并發癥風險。
(十)一次性使用球囊型冷凍消融導管:該產品由球囊型冷凍消融導管和手動回縮器套包組成,與該公司生產的冷凍消融儀配合使用,主要用于成人患者藥物難治性、復發性、癥狀性的陣發性房顫的治療。一次性使用球囊型冷凍消融導管采用特殊流體噴射裝置和球囊內壓力監測技術。特殊流體噴射裝置可保證球囊前半球表面溫度的均勻分布,實現有效消融;球囊內壓力監測技術可保證球囊穩定貼靠,實現球囊內部壓力穩定。該產品可有效降低消融過程中球囊因壓力波動而產生的彈跳移位風險,使更多陣發性房顫的患者受益。
(十一)經皮腎小球濾過率測量設備:該產品由主機、傳感器和固定貼組成,與該公司生產的瑞瑪比嗪注射液配合使用,主要用于評估患者腎小球濾過率。該產品采用漫反射校正和背景分離校正的熒光示蹤劑無創測量方法,通過皮膚表面獲取具有時變光學性質的熒光信號衰減數據,實現對腎小球濾過率的連續測量,具有操作簡單、無創、快速、準確和可重復測量等優點,使更多需要腎功能監測的臨床診療患者受益。
(十二)心臟脈沖電場消融儀和一次性使用心臟脈沖電場消融導管:心臟脈沖電場消融儀由主機和附件組成,附件包含交流電源線、腳踏開關、心電導聯線、等電位線。一次性使用心臟脈沖電場消融導管由電極、電極管、導管管身、手柄、連接器和連接電纜組成。上述兩個產品配套使用,利用高電壓脈沖產生的電場消融房顫,可使病變細胞發生不可逆的電穿孔而壞死或凋亡。該產品可實現對心肌組織的選擇性破壞,避免溫度傳遞導致的周圍組織損傷風險,使更多藥物難治性、復發性、癥狀性、陣發性房顫的患者受益。
(十三)經導管三尖瓣環成形系統:經導管三尖瓣環成形系統包括三尖瓣環夾系統和輸送鞘套件,其中三尖瓣環夾系統包括夾合部件、錨釘部件和輸送系統,輸送鞘套件包括輸送鞘和擴張器。該產品用于緩解患者的三尖瓣反流和心衰的臨床癥狀。適用于無需同期行左側瓣膜手術的孤立性重度三尖瓣反流伴有非嚴重的瓣環擴張或右心室擴大,有右心衰的臨床癥狀;無嚴重肺動脈高壓,無嚴重右心室/左心室收縮功能障礙,且經過指南指導藥物治療30天以上藥物治療療效不佳,經心臟團隊評估為不適合外科手術的65歲以上的高危禁忌患者。
(十四)消化道內窺鏡手術器械控制設備和一次性使用消化道內窺鏡組織鉗:該產品由電控單元、驅動裝置、操作手單元組成,與該公司生產的一次性使用消化道內窺鏡組織鉗配合使用,適用于食管、胃內鏡黏膜下剝離術中對病變組織進行鉗夾、提拉。該產品為國內首個消化內鏡整合型機器人,采用消化內鏡外掛柔性機械臂,通過主從控制模式實現末端執行器4自由度運動,精確控制夾取位置與方向,并對有重復夾取需求的組織進行提拉,確保手術視野清晰,降低手術風險。該產品具有設計簡潔、操作簡便、成本低廉等優勢,對推進我國消化道早癌早診早治,降低全社會消化道癌癥醫療負擔具有積極意義。
(十五)外周靜脈取栓支架系統:該產品由ClotTriever取栓鞘管和ClotTriever取栓支架組成,取栓鞘管組件包括鞘管、擴張器、預擴張器、裝載工具、大口徑抽吸注射器。該產品適用于有下述情況的下肢深靜脈血栓形成(DVT)的經導管血栓清除治療:(1)急性期髂股和股腘靜脈DVT;(2)亞急性期髂股靜脈DVT。
(十六)冠狀動脈介入手術控制系統:該產品由控制機柜、液晶顯示器、觸摸屏、控制盒、導絲與導管執行機構組成,適用于經皮冠狀動脈介入手術期間對導管和導絲的輸送與操作。該產品屬于支架遞送型機器人,采用隔室控制介入機器人手術系統、基于仿生學的導絲控制技術和柔性導絲阻力檢測技術。隔室控制介入機器人手術系統采用主從架構設計,具有低延時、高安全操作特點;基于仿生學的導絲控制技術模擬醫生手指導絲運動,具有小體積、高精度控制特點;柔性導絲阻力檢測技術實時獲取動態變化的受力信號,具有高靈敏、高穩定信息傳輸特點。該產品可有效提高經皮冠狀動脈介入手術的操作精度、穩定性和靈活性,使更多患者受益。
(十七)一次性使用壓力監測射頻消融導管:該產品由頭端、管身、手柄、線纜、鹽水接頭和光電混合插頭組成,與上海宏桐實業有限公司的心臟射頻消融儀配合使用,主要用于藥物難治性、復發性、癥狀性的陣發性房顫的治療。一次性使用壓力監測射頻消融導管通過內置光學壓力傳感器,實現臨床使用過程中壓力的實時監測和反饋,確保消融效果穩定性。該產品可有效降低術中導管與組織貼靠過緊造成蒸汽爆裂或貼靠不足引起消融不完全等風險,使更多陣發性房顫的患者受益。
(十八)心臟脈沖電場消融設備和一次性使用磁電定位心臟脈沖電場消融導管:心臟脈沖電場消融設備由主機、電源線、腳踏開關、夾式接地線、導管轉接盒、串口連接線等組成。一次性使用磁電定位心臟脈沖電場消融導管由心臟脈沖電場消融導管及連接尾線組成,其中導管由環形圈段、可彎段、主體段、取直器、控彎手柄及插座組成。上述兩個產品配套使用,利用高電壓脈沖產生的電場消融房顫,可使病變細胞發生不可逆的電穿孔而壞死或凋亡。該產品可實現對心肌組織的選擇性破壞,避免溫度傳遞導致的周圍組織損傷風險,使更多藥物難治性、復發性、癥狀性、陣發性房顫的患者受益。
(十九)心臟脈沖電場消融儀和一次性使用心臟脈沖電場消融導管:心臟脈沖電場消融儀由主機、腳踏開關及電源線組成。一次性使用心臟脈沖電場消融導管由主體管、放電電極、手柄、延長管和連接插頭組成。兩個產品配套使用,主要用于治療藥物難治性、復發性、癥狀性陣發性房顫。心臟脈沖電場消融儀輸出高壓脈沖信號,經一次性使用心臟脈沖電場消融導管傳遞至治療部位,通過輸出高壓脈沖電場能量,選擇性對目標治療區域心肌組織產生不可逆轉的電穿孔損傷,以實現肺靜脈電隔離達到對陣發性房顫治療目的。該產品利用脈沖電場的非熱效應原理對房顫進行治療,與傳統射頻消融及冷凍消融產品相比,可實現對心肌組織的選擇性破壞,有效避免溫度傳遞過程導致的周圍組織損傷等風險,使更多藥物難治性、復發性、癥狀性、陣發性房顫的患者受益。
(二十)經導管主動脈瓣膜系統:該產品適用于經心臟團隊評估無法耐受等待常規經導管主動脈瓣膜預裝時間的患者,且經心臟團隊結合評分系統評估后認為患有癥狀的、鈣化的、重度退行性自體主動脈瓣狹窄,不適合接受常規外科手術置換瓣膜,年齡≥70歲的患者。該產品為預裝式、可回收的經導管主動脈瓣膜系統,采用干瓣工藝制成,在提升臨床使用便利性的同時,減少了瓣葉長期處于壓縮狀態導致的瓣葉變形風險。
(二十一)一體式人工血管術中支架系統:該產品適用于Standford A型主動脈夾層的升主動脈、主動脈弓部置換和降主動脈支架象鼻術,采用一體式遠端免縫合固定技術,可縮短遠端循環時間,減少可能發生的并發癥。
(二十二)可降解耳鼻止血綿:該產品為多聚醚型聚氨酯海綿,由(DL-丙交酯-co-ε-己內酯)-氨酯共聚物組成,具有多孔層狀結構,對液體有一定的吸收容量,適用于鼻腔、中耳與外耳術后的暫時壓迫止血與支撐。
(二十三)血流導向密網支架:該產品適用于成人患者頸內動脈(巖骨段至末端)與椎動脈未破裂的囊狀寬頸(瘤頸≥4mm或瘤體/瘤頸比<2)或梭形動脈瘤;載瘤血管直徑2.0~6.0mm。該產品可完全推出微導管后再回收進微導管,支架與輸送系統機械鏈接,通過釋放手柄完成支架的機械解脫,實現支架的可控釋放。
(二十四)人工韌帶:該產品采用表面改性技術,在人工韌帶與軟組織接觸部分接枝聚苯乙烯磺酸鈉親水涂層,與骨道接觸部分通過礦化工藝涂覆羥基磷灰石涂層,植入后具有良好的固定效果。產品配合該公司不可吸收韌帶固定螺釘,適用于補償或加強損傷的膝關節交叉韌帶。
(二十五)血管外植入式心臟除顫電極導線和血管外植入式心臟除顫電極導線導入器:血管外植入式心臟除顫電極導線由電極導線、固定套管和分析儀電纜接口工具組成。血管外植入式心臟除顫電極導線導入器由胸骨下導入器和皮下導入器組成,胸骨下導入器包含手柄、不銹鋼穿隧桿、體外導桿,皮下導入器包含手柄、穿隧桿。上述兩個產品配套使用,與血管外植入式心律轉復除顫器組合構成血管外植入式心律轉復除顫器系統,放置在胸骨下,對發生或可能發生危及生命的室性心動過速的重大風險患者進行自動治療。該產品具有心臟和血管外抗心動過速起搏和停搏預防起搏功能,可減少經靜脈導線引起的相關并發癥,更好滿足患者臨床1.5T和3.0T場強的磁共振成像檢查需求。
(二十六)一次性使用磁定位壓力監測脈沖電場消融導管:該產品由頭端、管身、手柄、連接電纜組成,與本公司生產的心臟脈沖消融儀配合使用,主要用于陣發性室上性心動過速治療。一次性使用磁定位壓力監測脈沖電場消融導管通過對消融頭端結構的創新設計,實現高壓脈沖能量源在目標組織上的精準施加。該產品采用局部區域多電極設置方式,在提升消融頭端應對各種復雜微細組織結構適應性的同時,可實時顯示導管位置和頭端壓力監測值,有效提高手術效率、降低患者心臟穿孔并發癥。
(二十七)心臟脈沖電場消融儀和一次性使用心臟脈沖電場消融導管:心臟脈沖電場消融儀由主機、顯示器、腳踏開關、推車、連接線纜和電源線組成。一次性使用脈沖電場消融導管由導管和導管連接線組成,其中導管由環狀頭端、金屬電極、管身、標識管、手柄和連接器組成。兩個產品配套使用,主要用于治療藥物難治性、復發性、癥狀性、陣發性房顫。該產品采用脈沖電場的非熱效應原理進行房顫治療,與傳統消融產品相比,可實現對心肌組織的選擇性破壞,避免溫度傳遞導致的周圍組織損傷風險。同時,該產品還具有阻抗測量、心肌組織貼靠程度及導管與靜脈對齊程度的指示,進一步提高電機與目標組織的貼靠質量,使更多藥物難治性、復發性、癥狀性、陣發性房顫的患者受益。
(二十八)硬性接觸鏡護理消毒儀:該產品由底座、鏡片沖洗倉、防塵蓋、電泳解離倉、電源適配器組成。該產品與0.9%無菌氯化鈉溶液配套使用,用于硬性接觸鏡(氟硅丙烯酸酯硬性鏡)的清潔和消毒。
(二十九)經導管瓣中瓣系統:該產品由生物瓣膜、輸送器、球囊擴張導管、導管鞘套件、壓握器、充壓泵組成。生物瓣膜由牛心包瓣葉、鈷鉻合金瓣架、PET包覆物、縫線(PET、PTFE)組成。該產品適用于因先前置入的外科生物二尖瓣瓣膜衰敗(狹窄、反流或二者均存在)導致的癥狀性心臟病,且經心臟團隊結合評分系統評估為外科手術高風險或不適合接受常規外科手術的患者,進行經心尖的二尖瓣瓣膜置換。
(三十)含鎂可降解高分子骨修復材料:該產品由丙交脂-乙交脂共聚物(PLGA)、β-磷酸三鈣(β-TCP)、金屬鎂(Mg)組成,采用低溫增材制造技術及后處理制備而成。該產品適用于不影響骨結構穩定性的四肢骨缺損的填充和修復。
(三十一)主動脈弓支架系統:該產品包括主動脈弓主體支架系統和主動脈弓分支支架系統,與同公司主動脈覆膜支架破膜系統配合使用,適用于治療需要重建左鎖骨下動脈血運的Stanford B型夾層患者。
(三十二)經導管二尖瓣修復系統:該產品由夾合器及輸送系統、導管鞘組件組成。夾合器及輸送系統由夾合器、植入導管和可操控套管組成。導管鞘組件由導管鞘和擴張器組成,導管鞘包括可調彎鞘和手柄。該產品采用經皮方式,適用于經心臟團隊評估后認為存在外科手術高風險,且二尖瓣瓣膜解剖結構適合的退行性二尖瓣反流(MR≥3+)患者。
(三十三)血管外植入式心律轉復除顫器:該產品由植入式心律轉復除顫器和扭矩扳手組成,與血管外植入式心臟除顫電極導線組合成血管外植入式心律轉復除顫系統,放置在胸骨下,對發生或可能發生危及生命的室性心動過速重大風險的患者進行抗心動過速起搏、心臟復律和除顫自動治療。該產品具備心臟和血管外抗心動起搏、停搏預防起搏功能,與靜脈植入型心律轉復除顫器系統相比,可有效減少經靜脈導線引起的相關并發癥,更好滿足患者臨床1.5T和3.0T場強的磁共振成像檢查需求。
(三十四)數字PCR分析儀:該產品由溫控模塊、液滴生成模塊、光學模塊、運動控制模塊、電源模塊和軟件組成,主要用于對來源于人體血液樣本中白血病融合基因的核糖核酸進行定量檢測。該產品基于數字PCR檢測原理,通過注射振動技術將反應體系分割為數萬個液滴,每個液滴均可獨立完成PCR擴增反應。經PCR擴增反應后,有靶標核酸分子的液滴會產生熒光,無靶標核酸分子的液滴則不產生熒光,通過檢測每個液滴的熒光信號,計算出整個反應體系內的目標基因片段拷貝數,實現白血病融合基因的定量檢測。該產品與檢測試劑配套使用,為白血病診斷提供更精準的判斷依據,使更多患者受益。
(三十五)肺動脈取栓系統:該產品由FlowTriever取栓支架,Triever抽吸導管,FlowSaver血液回收裝置,大口徑抽吸注射器和FlowStasis可調節靜脈壓迫止血器組成。FlowTriever取栓支架采用“自膨脹圓盤”設計以捕獲血栓,Triever抽吸導管采用“大口徑”設計可快速抽吸血栓,FlowSaver血液回收裝置用于過濾以回收大口徑抽吸注射器抽吸的內容物。
(三十六)脊柱外科手術導航定位設備:該產品由機械臂系統、臺車、手術輔助套件和附件組成,適用于成人脊柱外科手術過程中手術器械和植入物的導航定位。該產品是國內首個采用微型機械臂技術的脊柱外科手術導航定位設備,可實現空間精確定位。與采用傳統多軸機械臂的同類產品相比,該產品可極大降低手術室及手術區域空間占用率,有效減少因機械臂碰撞引起的導航漂移等不良影響,具有安全、精準和高效等優勢。
(三十七)心臟脈沖電場消融設備和一次性使用心臟脈沖電場消融導管:該產品由主機、腳踏開關、電源線、消融導管尾線、標測尾線和心電信號連接線組成,與該公司的一次性使用心臟脈沖電場消融導管配合使用,主要用于治療藥物難治性、復發性、癥狀性、陣發性房顫。該產品為首個采用納秒級脈寬高壓脈沖電場實現肺靜脈隔離治療陣發性房顫的設備,利用高壓納秒脈沖發生器產生高壓脈沖電場,使病變細胞發生不可逆電穿孔效應,并采用脈沖信號測量生物阻抗,實現消融過程中組織損傷實時監測與反饋。與同類產品相比,納秒脈寬可使組織損傷更均勻,有效降低神經肌肉刺激,減少患者疼痛,使更多房顫患者受益。
(三十八)生物可吸收鎂合金加壓螺釘:該產品為加壓螺釘,由鎂基合金MgYREZr制成,產品無表面處理。該加壓螺釘材料的生物力學性能與人體骨骼相近,會在體內逐漸降解、吸收和代謝,被內源性新生組織所取代。
(三十九)生物型膝關節假體系統:該產品由股骨髁、脛骨平臺、脛骨平臺墊、定位柱和加壓桿組成。其中,股骨髁部件由符合YY 0117.3標準規定的鑄造鈷鉻鉬合金材料制成,內表面采用等離子噴涂純鈦涂層,涂層材料符合YY/T 0988.2標準的規定;脛骨平臺部件由Ti6Al4V ELI粉末經電子束熔融增材制造工藝制成,產品的化學成分和力學性能符合YY 0117.2標準的規定;脛骨平臺墊部件由含維生素E的高交聯超高分子量聚乙烯(牌號Chirulen? 1020EX)材料制成,符合YY/T 0811標準的規定;定位柱和加壓桿部件由符合GB/T 13810標準規定的TC4鈦合金材料制成。該產品作為非骨水泥型假體使用,適用于初次全膝關節置換。
(四十)雷帕霉素藥物洗脫冠狀動脈支架系統:該產品由預裝的藥物支架和快速交換型球囊擴張導管輸送系統組成。金屬支架由高氮無鎳不銹鋼制成,藥物涂層由雷帕霉素和乙交酯丙交酯共聚物(PLGA)組成,藥物劑量為100μg/cm。輸送系統由尖端、球囊、顯影標記、遠端內管、遠端導管、過渡導管、近端導管、抗變形段、導管座和親水涂層組成。 該產品適用于冠脈原發病變引致的缺血性心臟病患者,用以改善冠狀動脈腔內直徑,病變長度小于30mm,參考血管直徑為2.5-4.0mm。
(四十一)磁共振成像系統:磁共振成像系統由7T超導磁體、梯度系統、射頻系統、射頻線圈、工作站、生理信號門控系統、檢查床、電子柜組成,主要用于臨床核磁共振成像診斷。該產品采用深度學習技術,在7T高場磁共振成像系統基礎上增加了靜動態多通道發射平臺與多核成像功能,可提供頭部鈉圖像、四肢肌肉和肝臟的磷核波譜數據。該產品利用多通道與多核成像優勢,實現圖像的實時調節,可有效提高以中樞神經系統疾病為主的影像診斷效能,提高相應疾病治療水平。
(四十二)顱內動脈瘤輔助栓塞支架:該產品由顱內支架、輸送元件組成,部分規格含有輸送導管;輸送元件由輸送桿和導入鞘組成;輸送導管由微導管和塑形針組成。產品中支架是由單絲編織的兩端封閉的自膨式彈性結構,兩端喇叭張開角度和支架長度可調節,預期減少血管損傷及增強血管貼壁性,支架長度可調節預期可選擇性增加局部金屬覆蓋率。
(四十三)肺動脈取栓支架系統:該產品適用于有肺動脈主干或主要分支血栓,并存在高出血風險或溶栓禁忌的患者、經溶栓或積極的內科治療無效患者的急性高危肺栓塞或伴臨床惡化的中危肺栓塞的經導管血栓清除治療。產品使用了環間固定套設計,降低了取栓網籃的釋放、回撤過程中各網盤之間的形變傳導。
(四十四)全自動細胞形態學分析儀:該產品由玻片籃輸入輸出模塊、玻片取放模塊、顯微成像模塊、滴油模塊、玻片回收模塊等和軟件(主機應用軟件和PC應用軟件)組成,其中PC應用軟件包含:用戶交互界面、數據管理模塊、基于深度學習的細胞形態分析模塊。主要用于對來源于人體外周血液樣本中白細胞及有核紅細胞分類計數、紅細胞形態學分級和血小板數量估算。該產品基于光學顯微成像技術和深度學習圖像識別技術,通過對血細胞的快速定位與高清晰度圖像拍攝,獲取識別對象的邊緣、形狀、紋理和顏色等深層次抽象特征,實現白細胞、紅細胞與血小板形態學的精準分析。該產品可顯著提升外周血白細胞識別準確率及異常樣本篩查能力,使更多患者受益。
(四十五)X射線計算機體層攝影設備:該產品由掃描架、高壓發生器、X射線管組件、光子計數探測器、檢查床、激光定位燈、控制臺、限束器、選配件和附件組成。主要用于常規CT檢查,支持冠狀動脈CT血管造影和能譜檢查。該產品采用光子計數探測器替代傳統的積分型探測器,通過對探測器材料施加高偏置電壓,促使電流載體定向移動,形成電流脈沖,產生測量數據。與傳統CT相比,該產品具有更高的空間分辨率,可通過一次掃描獲得多個能量圖像,更好地滿足臨床影像診斷需求。
(四十六)經導管主動脈瓣膜系統:該產品為經股動脈入路,具有活動式定位件夾持原生主動脈瓣葉,可調彎輸送系統適配橫位心等復雜解剖結構。適用于經心臟團隊結合評分系統評估后認為患有有癥狀的、重度主動脈瓣膜關閉不全(重度主動脈瓣反流),或同時合并主動脈瓣狹窄,不適合進行常規外科手術置換瓣膜、年齡大于等于70歲的患者。
(四十七)焦深延長型人工晶狀體:該產品包括非預裝人工晶狀體(型號:AE2UV)和預裝人工晶狀體(型號:AE2UL22、AE2UL24、AE2UL28)。預裝型號由非預裝的AE2UV型人工晶狀體和植入器組成。其中人工晶狀體為一件式、可折疊、后房型人工晶狀體,改良L型襻,人工晶狀體主體部分和支撐部分主要由丙烯酸乙酯(EA)、甲基丙烯酸乙酯(EMA)聚合而成,添加交聯劑二甲基丙烯酸乙二醇酯(EGDMA)制成,采用等離子體表面處理工藝。人工晶狀體前后表面均為單焦設計,前表面采用高次非球面設計,后表面采用球面設計。該產品適用于成年人白內障摘除手術后無晶狀體眼的視力矯正,通過擴展焦深改善中視力以降低對眼鏡的依賴程度。
(四十八)心臟冷凍消融設備和一次性使用無菌冷凍消融探頭:心臟冷凍消融設備由主機、氬氣輸氣管路、氦氣輸氣管路和一次性使用無菌測溫器(選配)組成。一次性使用無菌冷凍消融探頭由探頭、手柄、連接管和測溫熱電偶組成。兩個產品配套使用,主要用于成人心臟病患者持續性房顫的治療。該產品利用氬氣節流后降溫現象,對消融心肌細胞進行快速冷凍,實現持續性心房顫動治療,具有快速復溫、真空隔熱、背側溫度反饋、操作簡單和安全性高等優點,使更多持續性心房顫動患者受益。
(四十九)交聯聚異丁烯非球面人工晶狀體:該產品為單件式后房人工晶狀體,可折疊,雙C型襻。人工晶狀體主體和支撐襻由疏水性交聯聚異丁烯材料制成,添加紫外吸收劑。光焦度范圍為+0.5 D~+34.0 D。人工晶狀體光學設計為單焦、非球面。該產品適用于成年人白內障摘除手術后無晶狀體眼的視力矯正。
(五十)焦深延長型人工晶狀體:該產品為單件式后房人工晶狀體,主體部分及襻采用疏水性丙烯酸酯材料。產品前光學區表面為非球面加衍射環設計,后表面為球面,采用多個衍射級次設計,實現焦深延長。適用于成年人白內障摘除手術后無晶狀體眼的視力矯正,通過擴展焦深改善中視力以降低對眼鏡的依賴程度。
(五十一)磁共振監測半導體激光治療設備、一次性使用激光光纖套件和立體定向手術計劃軟件:磁共振監測半導體激光治療設備由主機和配件組成。一次性使用激光光纖套件由醫用光纖導管組件和冷卻水管組成。立體定向手術計劃軟件由安裝U盤、密鑰組成。磁共振監測半導體激光治療設備與一次性使用激光光纖套件配合,用于對藥物難治性癲癇患者(局灶性發作,有明確的致癇區部位或明確的癲癇傳導途徑)的局部病灶進行激光治療。立體定向手術計劃軟件與磁共振監測半導體激光治療設備配合,用于頭部立體定向手術計劃制定。該產品可最大程度減少手術通路對正常腦組織的損傷,能更好保留認知功能。
(五十二)心臟電生理介入手術控制系統:該產品由執行器(含前端機械臂和前端驅動平臺、后端機械臂和后端驅動平臺)、操作器、工作站組成。產品與一次性使用電生理介入器械控制系統傳輸部件配合使用,輔助臨床醫師用于房顫導管射頻消融術期間,操控兼容的壓力監測射頻消融導管和鞘管。該產品采用遙操作系統執行電生理導管消融手術,替代術者在床旁手動操作導管和鞘管的傳統術式,產品在術中可實時圖形化導鞘關系,解決傳統手術中固定彎鞘管在三維標測系統內不可視的問題,手術安全性更高。
(五十三)前列腺癌磁共振圖像輔助檢測軟件:該產品由軟件安裝文件組成,功能模塊包括:確認模塊、設置模塊(含基于深度學習的前列腺配置),該產品是采用深度學習技術的人工智能醫療器械,可用于前列腺磁共振圖像的顯示、處理、測量和分析,對未治療的40歲及以上成人患者疑似前列腺腺癌病變進行輔助檢測,在臨床應用中可以提高醫生閱片質量,減少不必要的穿刺。
(五十四)胸腹主動脈覆膜支架系統:該產品包括胸腹主動脈主體覆膜支架系統、外周血管覆膜支架系統、主體延長支架系統、分叉型主體支架系統和髂延長支架系統。該產品用于胸腹主動脈瘤的腔內修復。適用的人群需滿足以下條件:良好的股、髂和上肢動脈入路;胸腹主動脈瘤近端錨定區直徑范圍為17-36mm,近端錨定區長度>25mm;內臟分支血管錨定區直徑范圍為6-13mm,長度≥15mm;腎動脈錨定區直徑范圍為4.5-9mm;長度≥15mm;遠端錨定區:如果遠端錨定區在髂動脈,則髂動脈直徑范圍7-25mm,長度≥15mm;如果遠端錨定區在主動脈,則主動脈直徑范圍12-36mm,長度≥20mm。
(五十五)一次性使用壓力監測心臟脈沖電場消融導管:該產品由導管和連接尾線組成,基于應變片原理的壓力傳感器設計,結合脈沖電場技術、磁場定位技術、鹽水灌注技術,與心臟脈沖電場消融設備配合使用,可用于房室結折返性心動過速和房室折返性心動過速的治療;與三維心臟電生理標測系統配合使用,可提供導管在心內的位置信息以及進行導管頭端和心壁之間觸點壓力的實時測量。該產品為室上性心動過速治療提供了更多選擇。
(五十六)分支型主動脈術中支架系統:該產品由帶有分支的支架及輸送器組成。其中支架由覆有PTFE膜的鎳鈦合金支架、不銹鋼連接套管、PET管狀滌綸布(帶標識線)及包膜縫線、人造血管、聚四氟乙烯的縫合線、包膜、包膜固定線組成。人造血管材質為PET、膠原、甘油。輸送器由大軟管、小軟管、釋放旋鈕等部件組成,其中釋放旋鈕通過釋放拉線分別連接支架的不同位置,可使支架分段釋放。該產品適用于Stanford A型主動脈夾層的外科開放手術治療。
(五十七)經導管主動脈瓣系統:該產品主動脈瓣的定位鍵設計預期可實現瓣膜精確定位與錨定;流出端大網孔設計預期可降低冠狀動脈患者后期冠脈再介入治療的難度;流入端菱形網孔高密度設計預期可提供良好的封堵效果。輸送器的可調彎設計和可旋轉設計預期可提高瓣膜定位和釋放的精確性。產品適用于經心臟團隊評估認為有癥狀、重度主動脈瓣反流(大于等于3級),不適合進行常規外科手術置換瓣膜、年齡大于等于70歲的患者。
(五十八)一次性使用無菌導尿管:該產品分為單腔、雙腔和三腔型。導尿管管身外表面含有聚賴氨酸涂層,基于聚賴氨酸與細菌細胞膜的電荷相互作用機制,以直接接觸方式發揮抑菌作用,減少細菌在導尿管表面的定植和生長。
(五十九)質子治療系統:該產品由加速器子系統和治療子系統組成,加速器子系統包括主加速器系統、能量選擇系統和射束傳輸系統,治療子系統包括360°旋轉束治療系統和治療計劃系統,適用于治療全身實體惡性腫瘤及特定良性疾病。該產品采用懸臂式機架的小型化設計,可節約質子設備的空間、提高治療效率。
(六十)植入式腦深部神經刺激器、植入式腦深部神經刺激電極導線和植入式腦深部神經刺激延伸導線:植入式腦深部神經刺激器與植入式腦深部神經刺激電極導線、植入式腦深部神經刺激延伸導線聯合使用,組成植入式腦深部神經刺激系統,該系統對伏隔核和內囊前肢進行刺激,用于難治性的中重度阿片類藥物成癮患者的防復發輔助治療。植入式腦深部神經刺激系統填補了物理性干預阿片類藥物成癮治療的技術空白,為阿片類藥物成癮患者的治療提供了更多選擇。
(六十一)腫瘤電場治療儀:該產品由主機、分線盒、一次性使用電極片、電源適配器、鋰離子電池、充電座組成,產生固定頻率的交變電場作用于腦部,適用于22歲及以上經組織病理學或影像學新診斷的幕上膠質母細胞瘤患者,在手術治療與放射治療后,與替莫唑胺(TMZ)聯合使用。該產品是首個用于該罕見病治療的國產產品,預期可提高患者治療的可及性。
(六十二)介入式左心室輔助設備和介入式左心室輔助導管泵套件:介入式左心室輔助設備和介入式左心室輔助導管泵套件聯合使用,用于高風險經皮冠狀動脈介入治療(PCI),為患有嚴重冠狀動脈疾病、左心室射血分數降低且血流動力學穩定的成人患者提供左心室輔助。
五、其他注冊管理情況
(一)境內第二類醫療器械注冊審批情況
2025年,各省級藥品監管部門共批準境內第二類醫療器械注冊41925項。其中,首次注冊14466項,占全部境內第二類醫療器械注冊數量的34.5%;延續注冊14060項,占全部境內第二類醫療器械注冊數量的33.5%;變更注冊13399項,占全部境內第二類醫療器械注冊數量的32%(見圖19)。2025年各省共注銷1857個注冊證。
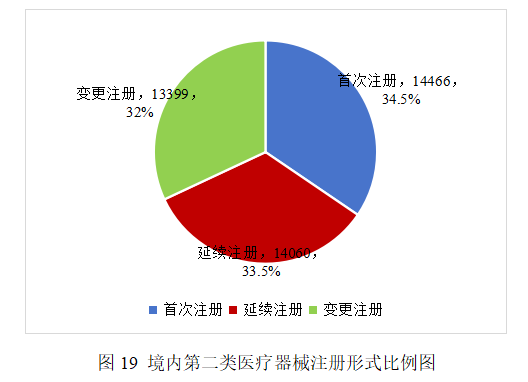
從注冊情況看,廣東、江蘇、北京、河南、浙江、湖南、上海、山東、湖北、河北10省(市)辦理境內第二類醫療器械注冊事項較多。
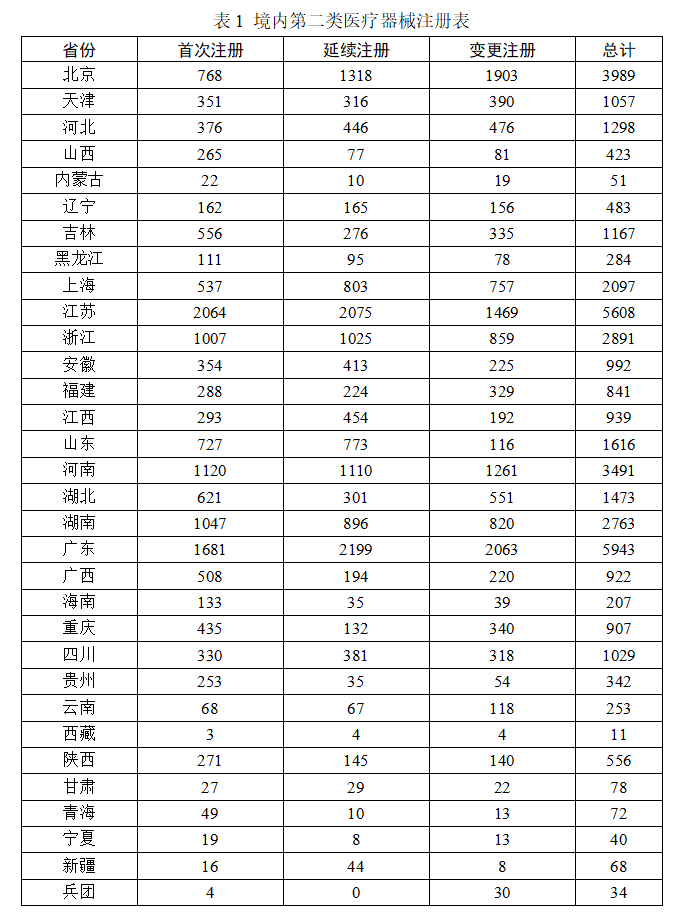
第二類醫療器械注冊具體數據見表1及圖20。
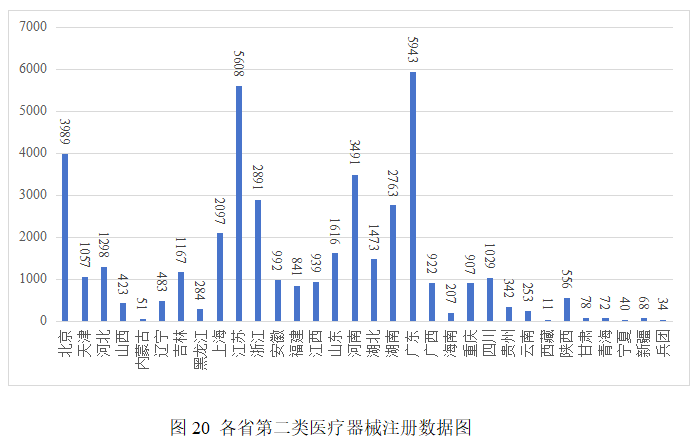
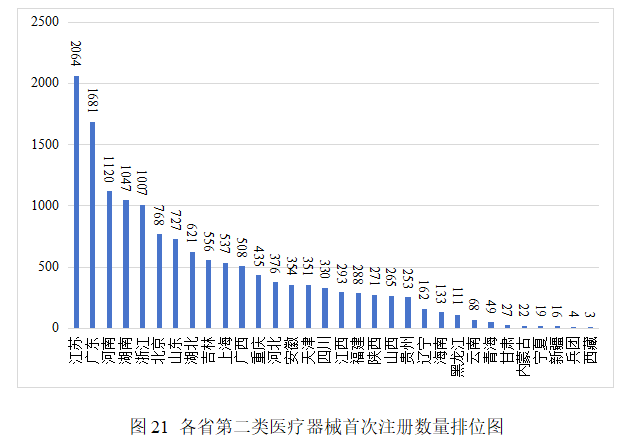
從首次注冊情況看,江蘇、廣東、河南、湖南、浙江、北京、山東、湖北、吉林、上海10省(市)首次注冊的境內第二類醫療器械數量較多。各省第二類醫療器械首次注冊數量排位圖見圖21。
(二)第一類醫療器械備案情況
2025年,國家藥監局依職責共辦理進口第一類醫療器械備案數量1826項。
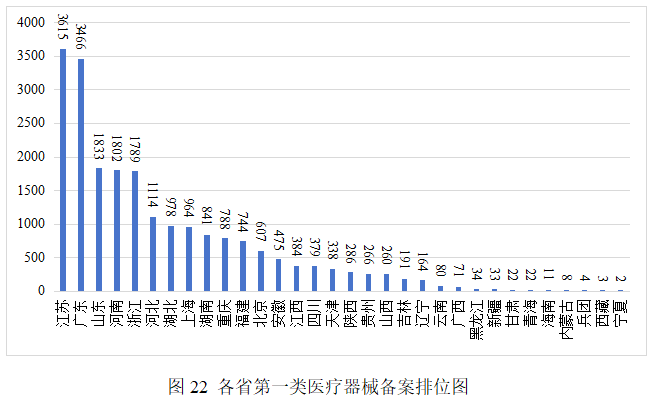
2025年,全國設區的市級藥品監管部門依職責共辦理境內第一類醫療器械備案數量21574項。其中江蘇、廣東、山東、河南、浙江是第一類備案數量前五的省份。各省第一類醫療器械備案排位圖見圖22。
(三)登記事項變更/變更備案情況
2025年,國家藥監局依職責共辦理進口第二、三類和境內第三類醫療器械變更備案6415項。
其中,境內第三類醫療器械變更備案4546項,進口第二類、三類醫療器械變更備案1869項。
各省級藥品監管部門依職責共辦理境內第二類醫療器械變更備案17741項。
(四)醫療器械臨床試驗機構備案情況
自2018年1月1日《醫療器械臨床試驗機構條件和備案管理辦法》頒布實施以來,全國共計1645個機構完成了醫療器械臨床試驗機構備案工作,2025年新增備案機構214個,比2024年增加14.29%。
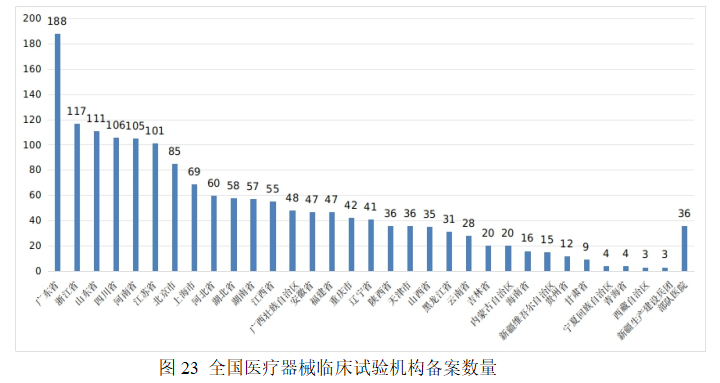
其中廣東、浙江、山東、四川、河南臨床試驗機構備案數量居全國前五名。全國醫療器械臨床試驗機構分布情況見圖23。
注:本報告的數據統計自2025年1月1日至2025年12月31日。
