2023年8月31日,國家市場監督管理總局發布《允許保健食品聲稱的保健功能目錄 非營養素補充劑(2023年版)》及配套文件解讀的公告,注冊證書“無有效期和無產品技術要求”的產品(以下簡稱為“雙無”產品),需要在5年過渡期內依據現行法律法規完成換證。2024年11月1日,市場監督管理總局發布《在產在售“無有效期和無產品技術要求”保健食品集中換證審查要點》,以集中規范在產在售“雙無”產品注冊證書。
- 哪些“雙無”產品需要重(補)做功能學試驗?
同時滿足以下兩個條件的“雙無”產品,需要按照要求重(補)做功能學試驗:
1)原功能學評價依據為《保健食品功能學評價程序和檢驗方法(1996版)》的;2)同時,產品功能屬于表1中所列的8大類保健功能的。
表1 八大類需要重(補)做功能學試驗的批件
序號 | 原保健功能聲稱 | 現保健功能聲稱 | 原功能學評價依據為96年版評價方法的,需重(補)做的功能試驗 |
1 | 免疫調節、增強免疫力 | 有助于增強免疫力 | 重做動物功能試驗 |
2 | 延緩衰老、抗氧化 | 有助于抗氧化 | 補做人體試食試驗 |
3 | 改善記憶、輔助改善記憶 | 輔助改善記憶 | 人體試食試驗使用韋氏記憶量表的,按現行規定重做人體試食試驗 |
4 | 抗疲勞、緩解體力疲勞 | 緩解體力疲勞 | 運動試驗為爬桿試驗的,按現行規定重做動物功能試驗 |
5 | 耐缺氧、提高缺氧耐受力 | 耐缺氧 | 重做動物功能試驗 |
6 | 減肥 | 有助于控制體內脂肪 | 重做功能學試驗 |
7 | 調節血脂(降低總膽固醇、降低甘油三酯)、輔助降血脂 | 有助于維持血脂(膽固醇/甘油三酯)健康水平 | 重做人體試食試驗 |
8 | 抗輻射、對輻射危害有輔助保護作用 | 對電離輻射危害有輔助保護作用 | 重做動物功能試驗 |
- “雙無”產品換證流程
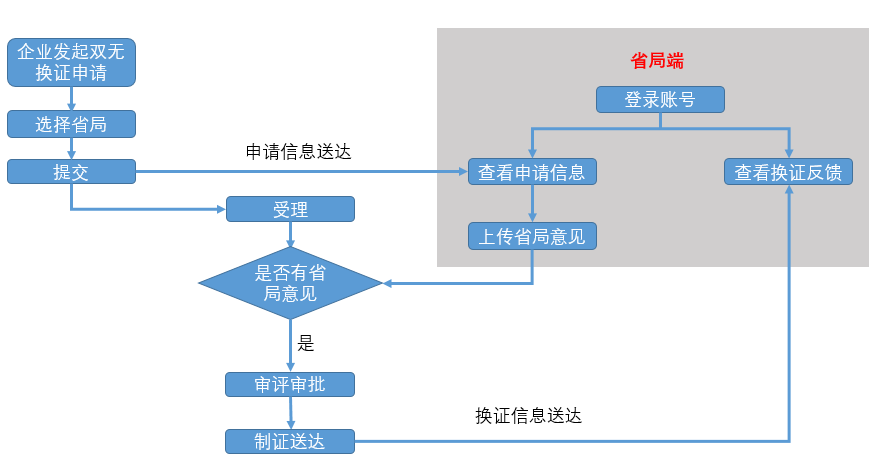
注:進口“雙無”產品無需省局出具換證意見。
建議注冊申請人事先向核發生產許可的省局提出【出具換證意見】的申請,拿到省局換證意見后,再在系統中發起“雙無”換證申請,以確保申報資料與省局意見中的附件相符(涉及配方、生產工藝、產品技術要求)。
不同省局出具換證意見的工作方案可能有所不同,根據廣東省于2024年12月12日發布的《關于做好在產在售“無有效期和無產品技術要求”保健食品集中換證工作的通知》,廣東省的工作流程如下:
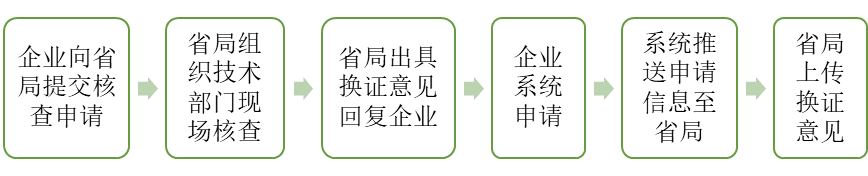
注:其他省份請了解相應省局的換證政策。
- “雙無”產品換證資料要求
國產“雙無”產品換證資料清單 | 進口“雙無”產品換證資料清單 |
|---|---|
1) 國產保健食品變更注冊申請表及注冊申請人對申請材料真實性負責的法律責任承諾書 | 1) 進口保健食品變更注冊申請表及注冊申請人對申請材料真實性負責的法律責任承諾書 |
2) 全部注冊人的有效主體登記證明文件復印件 | 2) 全部注冊人的有效主體登記證明文件復印件 |
3) 保健食品批準證書復印件及其相關變更、轉讓等批準證明文件復印件 | 3) 保健食品批準證書復印件及其相關變更、轉讓等批準證明文件復印件 |
4) 變更的具體事項、理由和依據 | 4) 產品生產國(地區)政府主管部門或者法律服務機構出具的注冊申請人為上市保健食品境外生產廠商的資質證明文件 |
除以上材料外,對于“無有效期和無產品技術要求”產品變更換證,還應提供相應材料: | 5) 產品生產國(地區)政府主管部門或者法律服務機構出具的保健食品上市銷售證明文件 |
1) 在全國范圍內,產品獲得有效生產許可的情況(列出核發生產許可的省級市場監管部門、SC號、核發日期、有效期截止日) | 6) 注冊人(境外生產廠商)在我國出入境檢驗檢疫部門的備案或注冊信息和產品進口信息 |
2) 注冊人對產品注冊證書不存在法律糾紛和歸屬爭議,以及換證產品不涉及執法案件尚未辦結情況的承諾書 | 7) 產品生產國(地區)或者國際組織與保健食品相關的技術法規或者標準原文 |
3) 變更產品名稱或保留產品名稱申請,以及商標注冊證復印件(無注冊商標的不需提供) | 8) 由境外注冊申請人常駐中國代表機構辦理注冊事務的,提交《外國企業常駐中國代表機構登記證》及其復印件;境外注冊申請人委托境內的代理機構辦理注冊事項的,提交經過公證的委托書原件以及受委托的代理機構營業執照復印件 |
4) 按照現行要求擬定的產品技術要求及制修訂說明、研究材料、試驗報告等材料 | 9) 變更的具體事項、理由和依據 |
5) 修改后的說明書樣稿及修訂說明 | 除以上材料外,對于“無有效期和無產品技術要求”產品變更換證,還應提供相應材料: |
6) 產品上市后人群食用安全性評價報告 | 1) 產品名稱變更申請或保留產品名稱申請,以及商標注冊證復印件(無注冊商標的不需提供) |
7) 需要的功能試驗報告、原輔料的合法來源證明等其他申請材料 | 2) 注冊人對產品注冊證書不存在法律糾紛和歸屬爭議,以及換證產品不涉及執法案件尚未辦結情況的承諾書 |
/ | 3) 境外銷售或進口銷售的最小銷售包裝實樣各2個,以及修改后的說明書樣稿及修訂說明 |
/ | 4) 產品上市后人群食用安全性評價報告 |
/ | 5) 按照現行要求擬定的產品技術要求,以及制修訂說明、研究資料、試驗報告等資料 |
/ | 6) 需要的功能試驗報告、原輔料的合法來源證明等其他申請材料 |
- 預估的“雙無”產品換證周期
從初期資料準備到官方審評審批,預期周期為1-3年。
