美國,是全球最大的消費市場,若醫療器械產品需要進入到美國市場,必須先通過FDA的認證。
一、 美國監管部門
1. 美國FDA
CDRH(Center for Devices and Radiological Health)醫療器械和放射健康中心:FDA負責醫療器械上市審批,負責審議上市前通告(510(K)/Premarket Notification)和上市前批準(PMA)的申請,以及所有未經批準、但將用于臨床試驗的醫療器械;
CBER(Center for Biologics Evaluation and Research )生物制品評價與研究中心:負責與生物制品相關的醫療器械的監管;
2. 監管法規
1976年 Food, Drug, and Cosmetic Act《聯邦食品、藥品和化妝品法案》(FDCA), Medical Device Amendment醫療器械修正案
1990年 Safe Medical Device Act《安全醫療器械法案》(SMDA)
3.醫療器械分類及注冊路徑
注冊路徑 | 適用產品 |
豁免 | 絕大部分Ⅰ類產品、少部分Ⅱ類產品 |
510(k) | 少部分Ⅰ類產品、大部分Ⅱ類產品 |
PMA | 少部分Ⅱ類產品、Ⅲ類產品 |
De Novo | 中低風險、無同類器械的新型產品 |
HDE | 用于治療罕見病或危及生命的疾病的特殊產品 |
EUA | 在公共衛生緊急情況(如疫情、生物威脅等)下,為快速審批未獲全面批準的醫療器械而設立的特別通道。 |
二、 注冊流程|周期
1.注冊流程
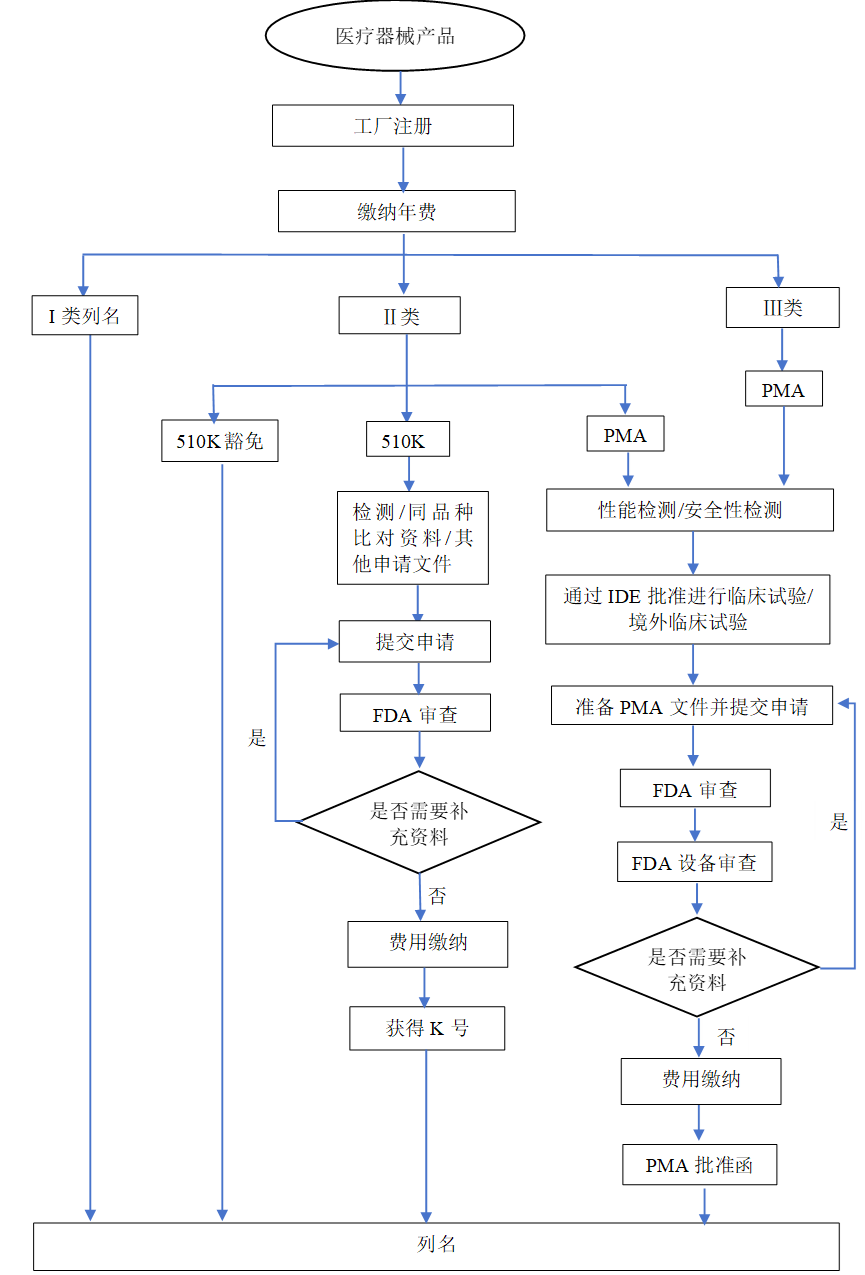
2.注冊周期
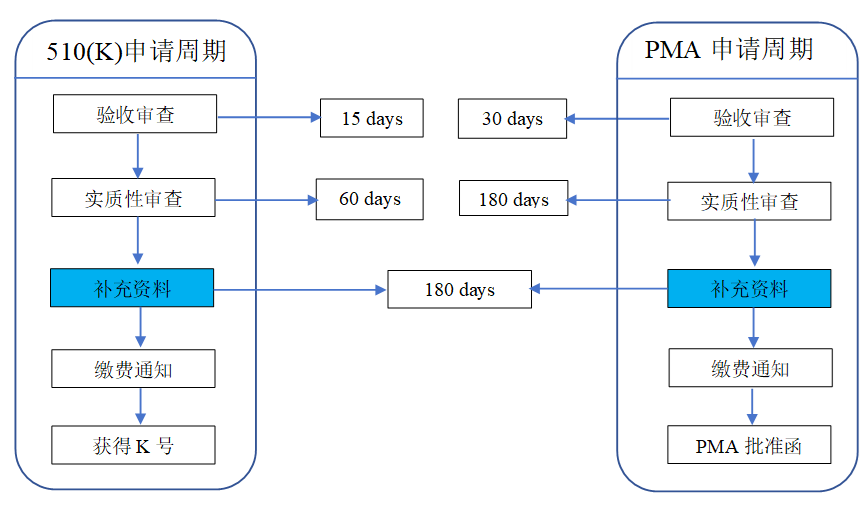
三、我們的服務
1. 監管策略與產品分類
產品分類與路徑確定: 準確確定產品在FDA的分類(I, II, III)并推薦最優的上市前提交路徑(如510(k), De Novo, PMA),規避戰略方向性錯誤。
監管藍圖制定: 量身定制從設計開發到最終批準的全周期監管策略和時間表。
2. 510(k) 提交服務
同類器械識別: 基于科學和法規依據,精準篩選和論證最合適的同類器械。
實質性等同論證: 系統地進行對比評估,并撰寫強有力的實質性等同論證報告。
全套510(k)文件編寫與匯編: 專業編寫包括摘要、器械描述、性能測試報告(生物相容性、滅菌、電氣安全、軟件驗證等)、標簽在內的全套文件,確保提交材料完整、合規。
3. De Novo 與 PMA 提交服務
臨床與技術支持: 為De Novo和PMA申請提供全方位的支持,包括試驗性器械豁免(IDE)申請、關鍵臨床試驗的設計與管理、復雜的數據統計分析和綜合性的技術文檔編寫。
與FDA的會議溝通: 協助準備與FDA的Pre-Submission等關鍵會議,提煉核心問題,準備會議材料,最大化溝通效率。
4. 質量管理體系(QMS)建立與審查
QSR 820合規: 協助您建立、實施和維護完全符合FDA 質量體系法規(21 CFR Part 820) 的質量管理體系。
模擬FDA審查: 提供模擬審查服務,識別體系漏洞,提前進行整改,助力從容應對FDA的現場檢查。
差距分析與體系優化: 對現有體系進行差距分析,并提供針對性的優化方案。
5. 產品列名
企業注冊與產品列名: 協助完成FDA的工廠注冊和產品列名。
6. 上市后監督與合規
不良事件報告: 指導建立符合醫療器械報告(MDR) 要求的體系,確保及時、合規地上報不良事件。
上市后監測計劃: 協助制定并執行上市后監測計劃,持續收集真實世界數據,滿足FDA對產品上市后的安全監控要求。
7. 美國授權代表
歐盟授權代表:提供具有符合要求且具有合規能力的授權代表服務。
四、證書模板
510K
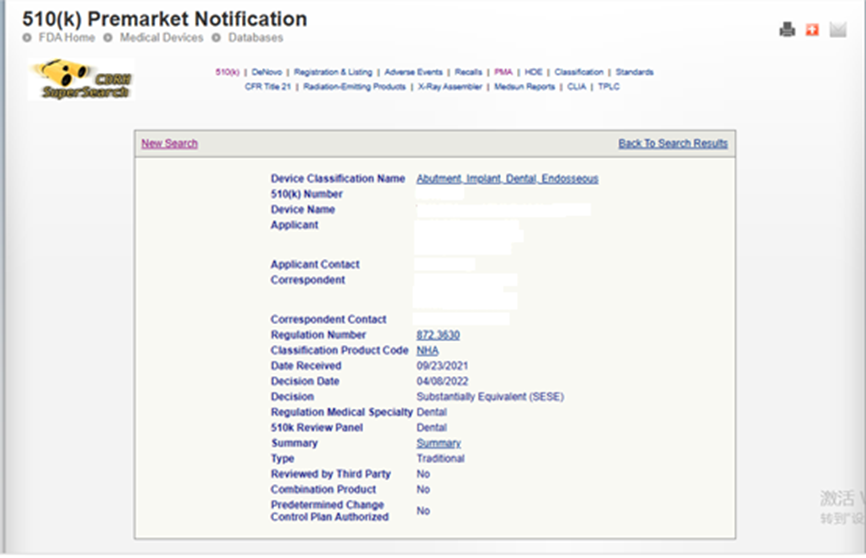
PMA