在歐盟市場“CE”標志屬強制性認證標志,不論是歐盟地區的企業生產的產品,還是其他非歐盟國家生產的產品,要想在歐盟市場上自由流通,就必須加貼“CE”標志,以表明產品符合歐盟《技術協調與標準化新方法》指令的基本要求。這是歐盟法律對所有產品提出的一種強制性要求,醫療器械也需要符合這個要求。當前,醫療器械須符合MDR法規,獲得相應的CE證書,加貼“CE” 標志,方可清關。
一、CE認證
1. 適用范圍
Ø CE認證:European Economic Area(EEA)歐洲經濟區,包括27個歐盟國家、三個EEA成員、瑞士和土耳其。
Ø 英國脫歐:大不列顛三島,進行UKCA認證,北愛爾蘭仍然認可CE。
2. 監管法規
Ø 歐盟醫療器械法規(法規(EU)2017/745),自2021年5月26日起適用。
Ø 體外診斷設備法規(法規(EU)2017/746),2022年5月26日起適用。
Ø 2023年3月15日歐洲議會和理事會條例(EU)2023/607,修訂條例(EU)2017/745和(EU)2017/746,涉及某些醫療器械和體外診斷醫療器械的過渡規定。該法規對醫療器械(MDR)條例(EU)2017/745 規定的過渡期進行了分階段延長。
3. 風險等級分類
醫療器械分類:按風險級別從低到高、分為:I類(普通1類/滅菌Is/測量Im/重復使用Ir)、IIa、IIb和III類,其中I類(普通1類/滅菌Is/測量Im/重復使用Ir)為低風險,III類為高風險。
IVD分類:按風險級別從低到高分為 A、B、C、D類。
MD | IVD | ||
風險等級 | 舉例 | 風險等級 | 舉例 |
Class III | 冠狀動脈支架、心臟瓣膜等 | Class D | 艾滋、新冠病毒檢測試劑 |
Class IIb | 縫合線、接骨螺釘等 | Class C | 血糖自測篩查等 |
Class IIa | 手術用手套、B超、輸液器等 | Class B | 妊娠自檢、尿液試紙等 |
Class I | 普通醫用檢查手套、病床、繃帶等 | Class A | 臨床化分析儀、標本容器等 |
4. 注冊語言
英語或其他公告機構認可的語言
二、注冊流程
1. 注冊要求
歐盟醫療器械分四類(I,IIa, IIb,III), 法規規定分類規則(附錄8),由制造商按照規則進行分類。低風險由制造商自我聲明,中高風險需要公告機構審核發放CE證書,高風險產品可能還需要主管當局或者歐盟對臨床進行審核。具體見下表:
分類 | 公告機構 | 技術文件審核 | 質量管理體系審核 | 主管當局 | 歐盟CECP* | 符合性聲明 |
I類(除滅菌、測量、重復使用) | 不需要 | 不需要 | 不需要 | 不需要 | 不需要 | 要 |
I類(帶滅菌、測量、重復使用) | 要 | 不需要-只確認滅菌、測量和重復使用部分 | 要 | 不需要 | 不需要 | 要 |
IIa, IIb(非植入) | 要 | 要-技術文件抽樣進行審核 | 要 | 不需要 | 不需要 | 要 |
Iib(植入)**、III類 | 要 | 要-技術文件不能抽樣 | 要 | 帶藥、動物源、人源、可吸收 | 見注釋 | 要 |
Iib有源輸注類,III類植入 | 要 | 臨床不能抽樣 | 要 | 帶藥、動物源、人源、可吸收 | 需要 | 要 |
2.CE證書申請流程
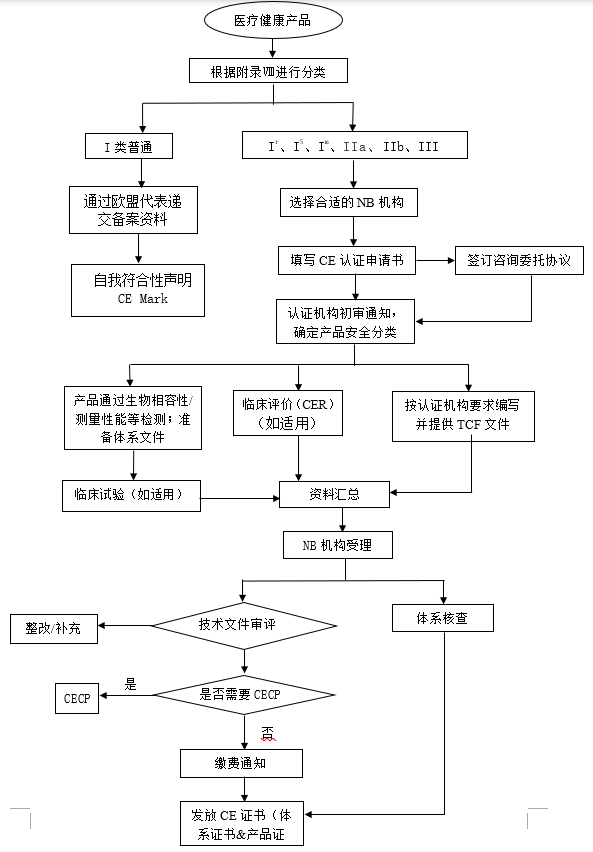
3. 公告機構(NB)CE認證(審核)流程
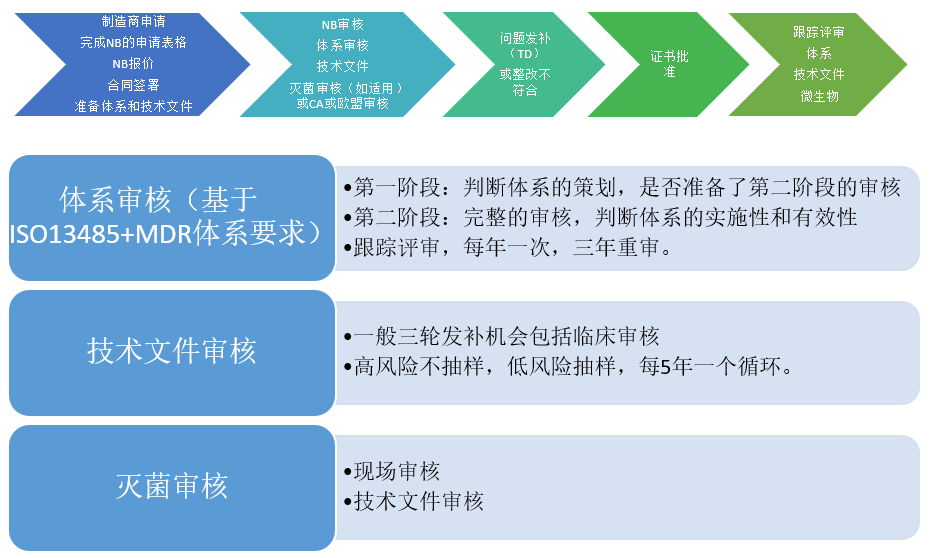
三、 我們的服務
1. 法規策略與數據缺口分析
產品分類與法規路徑確定: 準確判定產品在MDR/IVDR下的分類,并規劃最有效的符合性評價路徑。
數據缺口分析:系統評估現有技術文件、質量管理體系與MDR/IVDR要求的差距,提供清晰的改進路線圖。
2. 全面專業的臨床證據支持
臨床評價報告(CER)編寫:基于現有臨床文獻和/或等同性分析,撰寫完全符合MEDDEV 2.7/1 rev 4及MDR附錄XIV要求的CER報告。
臨床試驗設計與執行:提供從方案設計、倫理報批、中心篩選、項目監查到數據管理與統計分析的全流程臨床試驗服務,生成高質量、可接受的臨床數據。
上市后臨床跟蹤(PMCF)計劃與報告: 協助建立符合MDR要求的PMCF體系,規劃并執行PMCF研究,持續收集臨床數據,滿足法規對上市后監督的要求。
3. 技術文件(TCF)編制與優化
系統化文件構建: 系統化地整理和編寫所有必需章節,包括產品說明書、標簽、設計驗證報告、風險分析報告(符合ISO 14971)、滅菌驗證、軟件驗證(如適用)等。
專業審閱與提升:對現有文件進行審閱和優化,確保其結構完整、邏輯清晰、證據充分,能夠經受住公告機構的嚴格審查。
4. 質量管理體系(QMS)建立與優化
體系建立與整合: 協助建立全新的、符合MDR Annex IX Chapter I 和 ISO 13485:2016要求的QMS。
體系升級與優化: 將MDR的新要求(如上市后監督、供應商控制、UDI等)無縫整合到現有QMS中。
模擬審核與培訓: 提供公告機構審核前的模擬審核,并針對關鍵崗位人員進行法規和質量管理培訓,提升團隊整體合規能力。
5. 公告機構溝通與協調
充當溝通橋梁:負責與公告機構進行高效、專業的溝通,包括前期接洽、資料提交、問詢回復及審核安排,確保流程順暢。
6.歐盟授權代表(AR)
歐盟授權代表(AR):提供具有符合要求且具有合規能力的授權代表服務。
四、 證書模板
體系證書

產品證書


