一、香港醫療器械監管
1.醫療器械管理機構和法規
醫療器械管理部門:香港特別行政區政府衛生署下屬的醫療器械科(后續將由藥品醫療器械監督管理中心管理)
醫療器械監管法規:醫療器械行政管理制度(MDACS)及其配套法規。
2.定義與分類
醫療器械,意指制造商擬用于人體做以下一項或多項特定用途的任何器材、設備、工具、機器、器具、植入物、體外實際或校準器、軟件、物料或其他類似或有關物品(無論是單獨或以組合形式使用)。
醫療器械按風險等級分類,采用國際醫療器械監管論壇 (IMDRF) 的分類規則。
TIPs: 是否是醫療器械、分類等級可在官方網站小程序上進行判定
https://www.mdd.gov.hk/sc/mdacs/online-tools/index.html
3.本地責任人LRP
非香港制造商必須指定一名香港本地公司或個人作為本地責任人。
LRP要求:
(a) 須為在香港成立為法團的法人,或為在香港有商業登記的自然人或法人; 以及
(b) 須為醫療器械的制造商,或獲器械制造商支持以履行作為該器械的本地負責人所承擔的責任。
4.注冊制度
產品類別 | 表列制度 |
I類MD/A類IVD | X(不適用) |
II、III、Ⅳ類MD/B、C、D類IVD 已取得澳大利亞、加拿大、歐盟、日本、美國、中國、新加坡和韓國上市批件 | 通過遞交上述已上市證明文件進行表列 |
II、III、Ⅳ類MD/B、C、D類IVD 未取得澳大利亞、加拿大、歐盟、日本、美國、中國、新加坡和韓國上市批件 | 第三方機構(CAB)評核認證后,進行表列 |
二、注冊流程及周期
1.申報流程
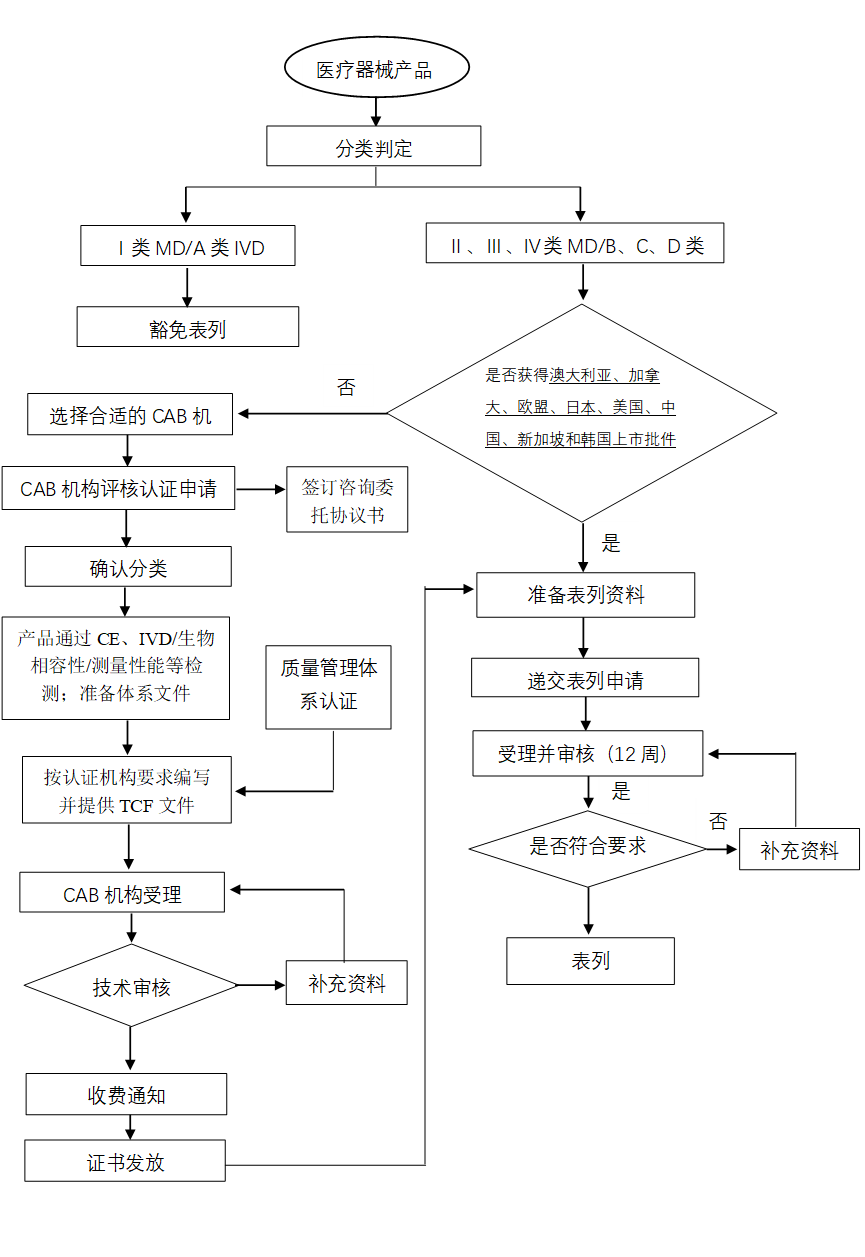
2.注冊申報費用
醫療器械表列:官方費用全免。
CAB評核:需收費,實際費用視具體CAB及產品而定。
3.注冊證有效期及延續
表列有效期5年。到期前12周至1年內遞交延續申請,過期重新申請表列。
三、我們的服務
1.產品評估與分類咨詢:準確判定產品的分類,并規劃最有效的符合性評價路徑。
2.本地負責人(LRP):提供具有符合要求且具有合規能力的本地負責人。
3.CAB機構評核認證
數據缺口分析:系統評估現有技術文件、質量管理體系與認證要求的差距,提供清晰的改進路線圖。
系統化技術文件構建:系統化地整理和編寫認證必須資料,包括產品說明書、標簽、設計驗證報告、風險分析報告(符合ISO 14971)、滅菌驗證、軟件驗證(如適用)等。
充當溝通橋梁:負責與CAB機構進行高效、專業的溝通,包括前期接洽、資料提交、問詢回復及審核安排,確保流程順暢。
4.表列申請
表列文件編寫:系統化地整理和編寫表列必須資料,確保其結構完整、邏輯清晰、證據充分,能夠經受住監管機構的審查。
充當溝通橋梁:負責與監管機構進行高效、專業的溝通,包括前期接洽、資料提交、問詢回復及審核安排,確保流程順暢。
四、表列證書模板

