ANVISA是什么?
巴西國家衛生監管機構Agência Nacional de Vigilância Sanitária (Anvisa)是隸屬于衛生部的自治機構,是巴西國家衛生監管體系(SNVS) 的一部分以及巴西統一衛生系統(SUS)的協調機構,其監管范圍覆蓋全國全境廣泛的產品和行業。該機構的核心職能是通過實施衛生監管控制,保障國民健康安全,具體涵蓋:
- 對受衛生法規管轄的產品(含原料)及服務的生產、銷售與使用環節進行衛生控制, 包括相關環境、流程、成分和技術;
- 在港口、航空口岸及邊境關卡開展進出口監督。
為什么要進行ANVISA認證?
ANVISA認證是食品上市流通的法定前提。ANVISA負責評估和批準食品的注冊,食品注冊批準須在《巴西聯邦政府官方公報》(Diário Oficial da União, DOU)公示后,方獲準在巴西市場營銷及分銷。注冊批準自DOU公告日起生效,有效期5年,屆滿前需提交重新驗證申請。
巴西新型食品申請適用法規
RESOLUÇÃO DA DIRETORIA COLEGIADA - RDC Nº 839, DE 14 DE DEZEMBRO DE 2023(第839/2023號決議:關于新食品和新成分的安全性證明和使用授權)
什么是新型食品和新型成分(Novos Alimentos, Novos ingredientes)?
所有在巴西沒有消費歷史的食品或成分都被歸類為新品,必須提交給 Anvisa 進行評估 。 自 1999 年 ANVISA 第 16 號決議(Resolução 16/1999)發布以來,衛生立法一直在考慮這種理解。 2023 年 12 月 14 日第 839 號決議(RDC 839/2023)撤銷了 1999 年第 16 號決議,并更新了新食品和新成分的監管框架,使新食品和新成分的含義更加清晰。
根據RDC839/2023號決議,新型食品和新型成分的定義是:
在巴西無安全食用歷史的食品和食品成分,這些食品和食品成分是從植物、動物、礦物、微生物、真菌、藻類中獲得的或合成的,包括但不限于:
(a) 具有新型或有意修改的分子結構;
(b) 由細胞培養物或組織培養物構成或以此類培養物為原料生產;
(c) 經過可導致顯著改變的生產工藝;
(d) 采用非傳統食品生產流程加工;
(e) 通過發酵、提取或選擇性濃縮獲得,并用于技術目的以改變食品的物理、化學、生物或感官特性,但未在IN211/2023規范性指令及其更新中作為食品添加劑列出;
(f)由工程獲得的納米材料構成;
(g)是傳統食品中使用的營養物質和非營養物質的來源;
(h) IN28/2018規范性指令或任何替代決議中未規定的食品補充劑成分;
(i) RDC22/2015 或任何替代決議中未規定的營養物質和其他腸內營養配方物質組成;
(j) RDC42/2011或任何替代決議中未規定的嬰幼兒食品的營養素組成;
(k)若用于其他食品,僅被授權用于食品補充劑和特殊用途食品的成分;或
(l) IN159/2022規范性指令或其他可能取代它的指令中未規定的用于制備茶葉或用作香料的植物物種。
ANVISA 進行安全性評估的目的是什么?
安全性評估是 ANVISA根據相關公司提交的技術科學文件分析新食品或成分安全性的行政程序。在這項分析中,ANVISA驗證了這種新食品或成分的制造過程不會引入或濃縮可能對健康產生有害影響的物質,或者食用適應癥不超過被認為的安全水平。
誰可以申請ANVISA認證?
ANVISA安全性評估請求通常由負責制造新食品或成分的公司提出,如果是外國公司,則由位于巴西的代表提出。
*需要注意的是,外國公司無法直接與ANVISA進行行政審批以獲取市場許可。外國公司必須有在巴西合法成立的合作公司,這些合作公司將對進口到巴西并在巴西境內銷售的產品負法律責任。
巴西新型食品認證資料要求
第839/2023號決議,對安全評估請求中要提交的文件進行了定義,新食品和新成分安全評估申請必須包含一份用葡萄牙語撰寫的技術科學報告 (RTC),其中包含以下信息:
|
*在決議中有比較詳細的各項資料的解釋和要求。同時在申請系統中,申請人可以訪問一份清單,該清單描述了根據安全評估申請的對象,為準備技術科學報告而必須提交的文件。
*其他申請資料參考文件:
- 第23/2019號指南(GUIA Nº 23, DE 23 DE JULHO DE 2019 - VERSÃO 1),該指南提供了支持安全評估申請的信息指導,包括被認為與執行證明使用安全性的過程相關的信息,對文檔提出建議,以及在此過程中必須指導的信息。該指南將進行更新,以符合RDC839/2023號決議的要求,但仍可用于協助檔案的指導。
- 第37/2020號指南(GUIA Nº 37, DE 2 DE SETEMBRO DE 2020 - VERSÃO 1),該指南表達了其對構成規范的要素的理解,主要針對在該機構認可的參考資料中沒有規格的成分和食品。
巴西新型食品申請流程
- 第一步:瑞旭整理整理、翻譯、編寫卷宗;
- 第二步:將完成的卷宗提交ANVISA,并進行評審;
- 第三步:通常需按照要求,回復ANVISA的問題或補充資料;
- 第四步:ANVISA將批準產品進口
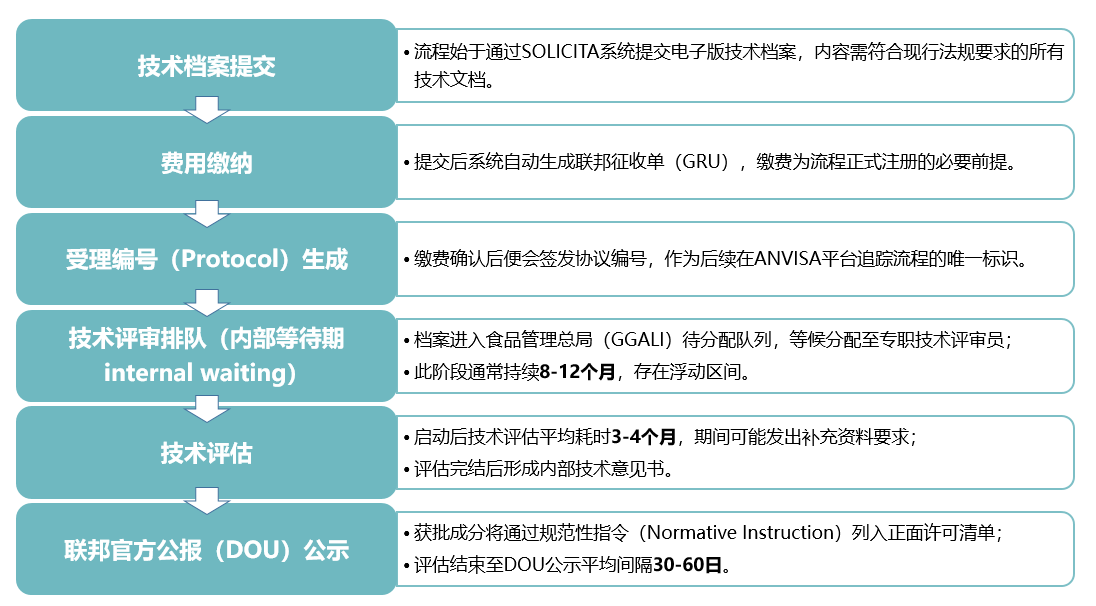
ANVISA安全性評估流程
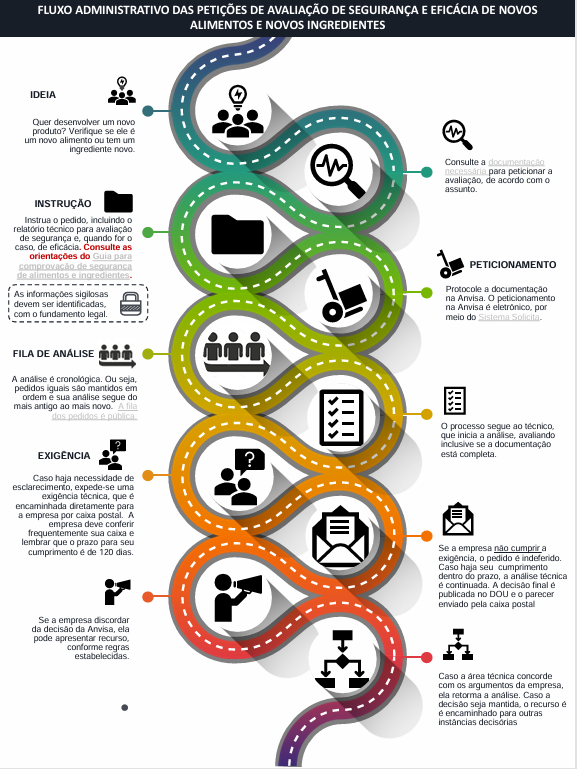
巴西新型食品認證周期
根據經驗,ANVISA新型食品審批流程周期從材料提交到聯邦官方公報(DOU)公示通常需要12到18個月的時間。但審批前等待時間及前述預審階段的持續時間存在顯著波動,主要取決于ANVISA內部工作負荷的變化。